大阪大学大学院医学系研究科
呼吸器・免疫内科学
Department of Respiratory Medicine and Clinical Immunology, Graduate School of Medicine, The University of Osaka
皮膚、粘膜を中心に急性炎症を反復する全身性疾患である。主症状(眼症状、再発性アフタ性口内炎、皮膚症状、外陰部潰瘍)と、副症状(関節炎、副睾丸炎、消化管病変、血管病変、中枢神経症状)が単独、複数で出現消退をくりかえす。腸管、血管、神経に主病変を有するものを特殊型ベーチェット病とする。好中球の機能亢進、T細胞の異常反応、血管炎、凝固亢進による血管障害がみられる。
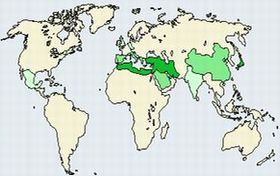
地中海沿岸、中東から東アジアにかけた地域に多く、「シルクロード病」ともよばれる。近年の本邦では、重症病変が減少傾向で、口腔内をはじめとした衛生状態の改善が免疫応答を変化させたためではないか、との仮説がある。
好発年齢は20~40歳、男女比は約1:1である。重症例は男性に多い。明らかな病因は未だ不明である。HLA-B51保有者が本症に罹患する相対危険率は6.7であり、遺伝的素因の関与が示唆される。細菌など微生物由来の熱ショック蛋白(HSP: heat shock protein)の関与も疑われている。
| 主症状 | |
|---|---|
| 眼症状 | ぶどう膜炎が典型で飛蚊症(ひぶんしょう、黒い点が動いて見える)、霧視(むし、霧がかかったように曇る)、羞明(しゅうめい、まぶしく見える)、眼痛など。前眼部ぶどう膜炎(虹彩毛様体炎)では前房に蓄膿が観察されることがある。後眼部ぶどう膜炎(網脈絡膜炎)は視力予後に関わり、繰り返すと失明のリスクとなる。 |
| 口腔粘膜症状 | 口内炎は境界鮮明な浅い有痛性潰瘍で、ほぼ必発の症状である。繰り返す、治りにくい、複数できる、しばしば大きいなどの特徴がある。 |
| 皮膚症状 | 結節性紅斑、皮下の血栓性静脈炎、毛嚢炎様皮疹、座瘡様皮疹がみられる。結節性紅斑や静脈炎はしばしば痛みを伴う。結節性紅斑は下腿にできることが多い。 |
| 外陰部潰瘍 | 境界鮮明、有痛性であることが多い。繰り返す、複数できるなどの特徴がある。 |
| 副症状 | |
| 関節炎 | 四肢の大関節(肘、肩、膝など)に好発する。関節破壊はまれである。 |
| 副睾丸炎 | |
| 消化管 | 回盲部に好発する。卵円型の深い潰瘍を形成し、腹痛、下血さらには穿孔に至ることがある。(消化管ベーチェット病) |
| 神経 | 急性型として、髄膜炎・脳幹脳炎が、慢性進行型として、小脳症状・脳幹萎縮・認知機能低下・性格変化などがみられる。(神経ベーチェット病) |
| 血管 | 血栓性静脈炎、(炎症性)動脈瘤、動脈血栓症がみられる。(血管ベーチェット病) |
血液検査では、疾患活動性の高い時期に、炎症所見(白血球数の増加、CRP・補体・免疫グロブリンの上昇、血沈の亢進)がみられる。疾患特異的な自己抗体などの検査はない。皮膚の被刺激性亢進を示す針反応は、本症に比較的特異的であり、採血の針のあとが腫れることで気づく場合がある。
消化管病変は下部内視鏡検査(大腸ファイバー)で精査する。神経ベーチェット病は、髄液検査で細胞増多・蛋白増加・インターロイキン6の上昇を、MRIで脳の実質変化を評価する。血管病変は、動脈瘤や血管狭窄をCTやMRIなどで精査する。これらの検査所見は、疾患活動性の高い時期には陽性となるが、疾患活動性が落ち着くと検出されない場合がしばしばあることに注意が必要である。
本邦の診断基準では4主症状、 5副症状の組み合わせで診断する。消化管病変、神経病変、血管病変が主であるものは、特殊型としてそれぞれ腸管ベーチェット病、神経ベーチェット病、血管ベーチェット病と診断する。
| 主症状 | |
|---|---|
| 口腔潰瘍 | 粘膜の再発性アフタ性潰瘍 |
| 皮膚症状 | 結節性紅斑、皮下の血栓性静脈炎、毛嚢炎様皮疹、座そう様皮疹 |
| 眼症状 | a) 虹彩毛様体炎、b) 網膜ぶどう膜炎(網脈絡膜炎)、a), b)を経過したと思われる虹彩後癒着、水晶体上色素沈着、網脈絡膜萎縮、視神経萎縮、併発白内障、続発緑内障、眼球労 |
| 外陰部潰瘍 | |
| 副症状 | |
| 関節炎 | 変形や強直を伴わない |
| 副睾丸炎 | |
| 消化器病変 | 回盲部潰瘍で代表される |
| 血管病変 | |
| 中枢神経病変 | 中等度以上 |
ベーチェット病は炎症の再燃を繰り返しながら、年齢とともに活動性の低下をみることもある。治療は重症度に応じるが、ぶどう膜炎や特殊型ベーチェット(血管ベーチェット、消化管ベーチェット、神経ベーチェット)で臓器病変が活動的な場合は中等量以上のステロイド、免疫抑制剤、生物学的製剤などが検討される。
粘膜皮膚病変にはコルヒチン(1-2mg/day)を使用、限局性の口腔内潰瘍や陰部潰瘍には外用ステロイドやスクラルファート液(アルサルミンなど)の局所療法、レバミピド(ムコスタR)溶解液うがいなども使用される。コルヒチンには関節炎の予防効果もあるが、関節炎がコルヒチンで治まらない場合は少量ステロイド、アザチオプリンなども使用される。
ぶどう膜炎に対しては急性期の高用量ステロイドとともに免疫抑制剤(アザチオプリン、シクロスポリン)が使用される。難治性ぶどう膜炎の場合は抗TNFα抗体(インフリキシマブ、アダリムマブ)が使用される。ぶどう膜炎は高度の視力障害をきたすことがあり、視力が低下する前に免疫抑制剤や生物学的製剤を導入することで視力予後の改善が期待される。
深部静脈血栓症は凝固亢進より血管炎の結果と考えられステロイドと免疫抑制剤(アザチオプリン、シクロスポリンなど)、難治性の場合は抗TNF抗体(インフリキシマブ)が考慮される。出血リスクが低い場合は抗凝固薬を追加してもよい。
消化管病変に対して5-ASAやアザチオプリンとともにステロイドが使用されるが、難治性では抗TNFα抗体(インフリキシマブ、アダリムマブ)が使用される。
神経ベーチェット病には急性型と慢性型があり、急性型には中等量以上のステロイドを用いコルヒチンやアザチオプリンを追加することもある。シクロスポリンによる誘発もあり同剤使用中であれば中止する。慢性型にはMTXを開始し場合によってはインフリキシマブを追加併用する。
| 包括的原則 | |
|---|---|
| A | ベーチェット病は再発と寛解を繰り返し、臓器障害や生命を脅かすことがあるが、症状は時間とともに改善することもある。 |
| B | 治療目標は不可逆的な臓器障害を防ぎ、健康関連QOLを最大限に高めることである。 |
| C | 臓器障害は疾患経過を通して評価し、適切な検査で類似疾患を除外する。 |
| D | 治療は、年齢、性、臓器障害の種類と重症度、疾患期間、患者希望に応じて個別化する。 |
| E | 最適な治療に、多職種連携、患者教育、共同意思決定、治療遵守、生活習慣改善が必要。 |
| 推奨(括弧内は同意度) | |
|---|---|
| 粘膜 皮膚 |
1 再発性の粘膜皮膚病変の第一選択薬はコルヒチン。コルヒチンに難治性や不耐性では、アプレミラストやTNFα阻害薬を検討する。(9.5) 2 口腔潰瘍や性器潰瘍の治療はグルココルチコイド(GC)などの局所療法を用いる。全身性GCの慢性使用は避ける。(9.0) |
| 関節 | 3 急性関節炎の第一選択治療薬はコルヒチン。再発や慢性では免疫抑制剤を検討する。(9.4) |
| 眼 | 4 ベーチェット病ぶどう膜炎の全患者は、臨床的および血管造影上の寛解誘導と維持を目的とし免疫抑制療法を行う。後眼部炎症で視力障害をきたす炎症は、抗TNFα抗体、特にインフリキシマブ(IFX)を他の免疫抑制剤と併用する。GC単剤治療は行わない。(9.7) |
| 動脈 | 5 肺動脈瘤および末梢動脈瘤には、高用量GCとIFXが推奨される。シクロホスファミドも代替薬。GCは徐々に減量し、免疫抑制剤、特に抗TNFα抗体は維持で継続する。(9.8) 6 必要に応じて、迅速な薬物療法開始後、血管処置を遅らせるべきではない。重篤な出血リスクの高い肺動脈瘤は開胸手術より塞栓術を推奨。(9.7) |
| 静脈 | 7 脳静脈洞を含む深部静脈の急性血栓症の治療には、GCと免疫抑制剤、特に抗TNFα抗体の使用を検討し、免疫抑制剤は維持として継続する。(9.7) 8 出血リスク低く肺動脈瘤合併が除外されるなら抗凝固薬を追加してよい。(8.7) 9 視力障害を伴う頭蓋内圧亢進を伴う脳静脈洞血栓症は、外科的介入を速やかに検討する。(9.0) |
| 消化管 | 10 消化管病変の診断、重症度評価、治療は、内視鏡検査に基づく。(9.5) 11 消化管病変には、5-ASAやアザチオプリンを、GC併用または非併用で使用する。重症または難治性では抗TNFα抗体の使用を検討する。(9.6) |
| 神経 | 12 活動性の実質神経系病変は、高用量GCおよび免疫抑制剤(好ましくはIFX)の投与を開始すべきである。GCは徐々に減量し、免疫抑制剤は維持で継続する。(9.8) |
包括的原則の補足
長期的には免疫抑制剤の減量中止を目指すべきだが、寛解となっても臓器再発や新たな臓器病変には注意し、感染症などの合併症との区別が大切。家族歴や若年発症ではトリソミー8関連自己炎症性疾患やA20ハプロ不全症などの単一遺伝子模倣疾患を除外する。
リウマチ専門医、皮膚科医、眼科医、神経内科医、消化器内科医、血管外科医など多職種連携によるアプローチは、各症状の診断、重症度評価、治療、経過観察に重要である。
良好な口腔衛生、健康的な食事、運動などの生活習慣の改善も重要。患者には口腔衛生状態の悪さと口腔潰瘍の増加との関連性について説明する。禁煙を奨励するが、禁煙によって一時的に口腔潰瘍が増加する可能性がある。
各臓器傷害への推奨の補足
粘膜皮膚
患者によって内服薬より、時折の病変は局所薬を好む場合がある一方、重症への進行リスクを避けるため忍容性の高い投薬を好む専門家もいる。コルヒチンは外陰部潰瘍や結節性病変に対して、有効性、忍容性、低コストで、主要臓器病変がない活動性粘膜皮膚症状に第一選択。口腔潰瘍には外用GCや口腔衛生などの局所療法が推奨される。高力価の局所GCが好ましいこともあるが長期間使用すべきではない。
活動性外陰部潰瘍は感染症を合併する可能性があり、局所GCと局所抗生物質の併用が好ましい場合がある。重度の外陰部潰瘍は治癒促進のため低用量GCを短期投与が試みられる。丘疹膿疱性病変は、尋常性痤瘡に使用される局所療法、重症はレチノイドで治療することがある。粘膜皮膚病変のみでは全身性GCは推奨されない。厄介な粘膜皮膚病変ではアプレミラストが好まれる。TNFα阻害薬(ADAやIFX)も代替薬。IL-12/23阻害剤ウステキヌマブの有効例もある。
関節
関節炎はコルヒチンで良好なRCTの報告があり、有効性、忍容性、コストに基づきコルヒチンが第一選択。コルヒチン抵抗性ではアザチオプリンやTNFα阻害剤などを試す。アプレミラストも選択肢。低用量経口GC、GC関節内注射、NSAIDsも、関節炎発作中に試すことができる。コルヒチン抵抗性の一部は免疫抑制剤よりも低用量GCの継続投与が好ましい場合がある。ウステキヌマブの前向き単群試験で関節炎減少の報告もある。
眼
ぶどう膜炎を迅速に抑えるためPSL 0.5~1 mg/kg/日で開始。mPSLパルスは、パルスなしと比べて視力を改善する。一方、IFXはmPSLパルスより優れた有効性を示す。局所GCと硝子体内注射は、免疫抑制剤に加えて急性増悪時にも使用できる。GCに加え免疫抑制剤は活動性ぶどう膜炎を伴うBS患者全員に重要で、重症度と予後因子により選択する。重度の硝子体混濁や眼底蛍光血管造影で広い毛細血管漏出の所見と視力障害を伴う後部ぶどう膜炎はIFXやアダリムマブなどTNFα阻害薬を早期に使用する。軽症はアザチオプリン、CyA、MMFで治療できるが、寛解しない又は再発では生物製剤へ切り替えや追加を行う。トシリズマブもIFXやADAと同様の視力、嚢胞様黄斑浮腫、硝子体炎スコアの改善の報告がある。
主要臓器病変の治療目的は、速やかに寛解をもたらすことで、ぶどう膜炎患者にとって視力維持のために非常に重要である。血管造影で漏出が長期的な再発と関連があるため、寛解の定義は血管造影による寛解を含むよう拡大されている。ぶどう膜炎の再発を防ぐために生物製剤の長期使用が合意されている。中止を試みる際は血管造影で寛解を確認し、徐々に減量する。多くの専門家は免疫抑制剤の長期間継続を推奨する。
動脈
動脈病変のある患者はGCを直ちに開始し、通常は1gのmPSLパルスを3連日後、経口PSL 1mg/kg/日から開始、6~12ヶ月で漸減中止する。動脈病変は高用量GCに加えてIFXが第一選択。生命を脅かす動脈病変を伴う難治例は、投与量を増やす、別のTNFα阻害薬に切り替える、またはIFXにシクロホスファミド追加が報告されているが毒性に注意。維持はアザチオプリンなどの従来の免疫抑制剤よりもTNFα阻害薬が優先。動脈病変で免疫抑制剤をいつ減量中止するかデータはなく、少なくとも5年継続治療すべきと提案された。
サイズが大きく有症状の末梢動脈瘤や大動脈瘤には緊急の血管処置が必要になる。グラフト挿入、結紮、バイパス手術などの選択は、動脈瘤の大きさや位置、施設の経験による。血栓症リスクが高いため、合成グラフトは静脈グラフトよりも優先される。
静脈
静脈血栓症は、下肢の静脈潰瘍を伴う血栓後症候群、バッド・キアリ症候群における門脈圧亢進症、持続的な心内血栓症が存在する場合の心内膜線維症、脳静脈洞が広範囲に侵されると失明につながる頭蓋内圧亢進症を引き起こす可能性がある。したがって、GCと免疫抑制剤による迅速な治療が必須で、動脈病変と同様に、mPSLパルスから始まる高用量レジメンは、大静脈の急性血栓症、心内血栓症、および視力障害を引き起こす脳静脈洞血栓症において好ましい場合がある。下肢深部静脈血栓症の患者には、中等度の初期投与量で十分な場合がある。免疫抑制剤、できればTNFα阻害薬をGCとともに直ちに開始する。血管病変に対してはシクロホスファミドよりもIFXを支持するRCTや、従来の免疫抑制剤と比較して生物製剤が良好な結果を示す2つの観察比較研究がある。
脳静脈洞血栓症は大多数の症例で再発のない軽症であるものの、高用量GCや免疫抑制剤によるにもかかわらず、視力障害を引き起こす頭蓋内圧亢進をきたす可能性がある。このような患者では不可逆的な視力喪失が急速に進行する可能性があり、腰椎腹腔シャントや開窓術などの外科的介入を速やかに検討する。
2018年以前の2つの後向き研究は、抗凝固薬が静脈血栓症の再発リスクを低下させないことを示している。また、ADAと従来の免疫抑制剤の比較は、抗凝固薬を追加してもどちらのグループでも転帰が改善しなかった。他の後向き研究では、免疫抑制剤に抗凝固薬の追加で再発率と血栓症の予防に関して相反する結果がある。
消化管
内視鏡検査は、消化管病変の診断、クローン病、潰瘍性大腸炎、NSAIDs潰瘍、結核などの鑑別、積極的治療を要する重症疾患の判定、寛解を確認するために必要である。
アザチオプリンまたは5-ASA誘導体は、軽度から中等度の消化管症状のコントロールに十分である可能性がある。急性増悪時は、PSL 0.5~1mg/kgで開始する。消化管症状がひどく、出血や穿孔のリスク患者では、GCは作用発現が速いため有益である可能性がある。しかし、高用量GCでは穿孔の兆候を見過ごさない。火山型潰瘍、深部潰瘍、2cmを超える潰瘍などは出血や穿孔の高リスクでTNFα阻害薬を勧める。重度の出血、穿孔、または閉塞のため手術が必要になることがある。周術期合併症の予防に効果的な免疫抑制が重要である。
神経
重度の増悪はmPSLパルス後、経口PSL 1 mg/kg/日で開始。数日間にわたって回復不良ではパルスを最大 7~10 回繰り返すことができる。観察研究ではIFXで良好な反応がある。
急性神経系障害は障害リスクが高く、TNFα阻害薬が第一選択になった。TNFα阻害薬はアザチオプリンと比べGC減量が速かった。アザチオプリンとTNFα阻害剤の併用も検討される。トシリズマブは他の治療法に抵抗性の一部に有益性を示唆する非比較データがある。CyAの神経系のリスク増加がメタ分析で示され、神経系患者へのCyAは推奨されない。
トシリズマブ、ウステキヌマブ、JAK阻害剤などのオプションは、小規模な研究またはバイアスのリスクが高い研究しかないが、推奨事項の治療に抵抗性で、証拠のある選択肢がなくなった場合に言及されている。
神経型ベーチェット病は臨床的特徴と治療反応性から急性型と慢性型に分けられそれぞれ治療法が異なる。脳実質に起因することが多いが上矢状静脈洞血栓症などの血管病変によるものもある。小脳、脳幹、大脳基底核の障害に基づくことが多く、多発性硬化症と似る。国内専門6施設での20年間のデータを後ろ向きコホート調査が公表されている(平成25年12月ベーチェット病に関する調査研究班 研究代表者 石ケ坪良明)。
発熱や頭痛を伴った髄膜脳炎の型をとるが、片麻痺や脳神経麻痺など脳局所徴候を来すことが多い。MRIのT2強調やFLAIRで高信号を呈す。脊髄液は細胞数と蛋白の上昇とIL-6の著明な上昇を伴う。ステロイドによく反応するが自然軽快することもある。シクロスポリンで誘発されることがる。
1~3のすべてを満たすものを急性型神経型ベーチェット病と診断する。中枢神経系感染症の除外が必要。また、シクロスポリンで誘発される亜型が存在する。
(ベーチェット病診療ガイドライン2020から。括弧内は、証拠レベル、同意度、推奨度)
| ・急性型の40%は再発し、大発作では後遺症を残すことがある。慢性進行型は進行すると予後不良である。神経型ベーチェット病の診断基準を満たすものは中等度以上の中枢神経病変に含める。(3, 4.8, A) |
| ・シクロスポリンが使用されている場合は中止する。(3, 4.9, A) |
| ・初回発作が生じたらすぐにコルヒチン(1-2mg/day)を開始し5年間は継続する。(3, 4.5, B) |
| ・MTX、シクロフォスファミド、AZPの再発予防効果はコルヒチンより劣ると考えられ、これらの積極的投与は行わないことを提案する。(3, 4.2, C1) |
| ・急性期はPSL 20mg/日以上を投与し効果不十分ではステロイドパルスを含む大量投与を行う。(3, 4.5, B) |
| ・急性期の治療でPSL中等量以上が効果不十分なときインフリキシマブ併用を提案する。(5, 4.4, C1) |
| ・コルヒチンを使用しても再発する場合はインフリキシマブを考慮することを提案する。(5, 4.2, C1) |
| ・急性型症状が治まり検査所見が改善しPSL10mg以下になったら神経学的所見と頭部MRIを評価、脊髄液IL-6を測定し17pg/mL以上であれば慢性進行型を疑う。(3, 4.6, B) |
ステロイド抵抗性で持続進行の経過を辿り、精神症状(認知症、人格変化)、体幹失調、構語障害などの症状やMRIで中脳から橋にかけての脳幹や小脳の萎縮などが見られる。急性型神経型ベーチェット病の発作出現後数年して精神症状などが徐々に出現することがある。HLA-B51陽性率が高く、男性、喫煙者が多い。髄液中のIL-6が数ヶ月以上持続して高値となる。
1~3のすべてを満たすものを慢性型神経ベーチェット病と診断する。参考所見として慢性進行型では男性、喫煙、HLA-B51の頻度が高い。
(ベーチェット病診療ガイドライン2020から。括弧内は、証拠レベル、同意度、推奨度)
| ・先行症状としての急性型症状の発現は約90%あるが、必発ではない。(3, 4.8, A) |
| ・慢性進行型の治療はできる限り髄液IL-6を17pg/mL以下に下げるよう努力する。(3, 4.6, B) |
| ・まずMTX単独で治療し、神経症状改善なく髄液IL-6が17pg/mL以下にならない場合は速やかにインフリキシマブ(5mg/kg、 0、2、6週、以降8週間隔。効果不十分では10mg/kgに増量可)を導入する。(2b, 4.6, B) |
| ・慢性進行型の治療は髄液IL-6低値維持と症状進行がなく、MRIで脳幹などの萎縮の進行がないことを目標とする。(2b, 4.7, B) |
| ・治療内容が固まるまで頭部MRIや髄液IL-6検査は適宜行い、その後MRIは少なくとも年一回、髄液IL-6もできる限り年一回測定する。(3, 4.7, B) |