肝細胞死・肝星細胞微小環境研究グループ
グループリーダー:齋藤義修
コンセプト:肝細胞死を起点に、肝星細胞を中心とする微小環境との相互作用から、線維化・発癌へ至る慢性肝疾患の病態連鎖を解明し、トランスレーショナルリサーチ(橋渡し研究)で新規治療創出を目指す。
本グループは、肝細胞死(アポトーシスおよび非アポトーシス型)を起点に、炎症・免疫応答、肝星細胞を中心とする微小環境の変容、線維化、肝発癌へと連なる慢性肝疾患の病態連鎖を統合的に解明します。単一細胞RNA解析(single-cell RNA-seq)・空間的トランスクリプトーム(spatial transcriptomics)・クロマチン解析に、マウスモデル、オルガノイド、共培養系を組み合わせ、肝星細胞サブポピュレーションの機能、細胞間シグナル、転写制御ネットワークを明らかにします。さらに臨床検体(生検・切除組織・血液)で検証し、バイオマーカー開発と治療介入の検証を通じて、橋渡し研究(Translational Research)による新規予防薬・治療薬の創出を目指します。
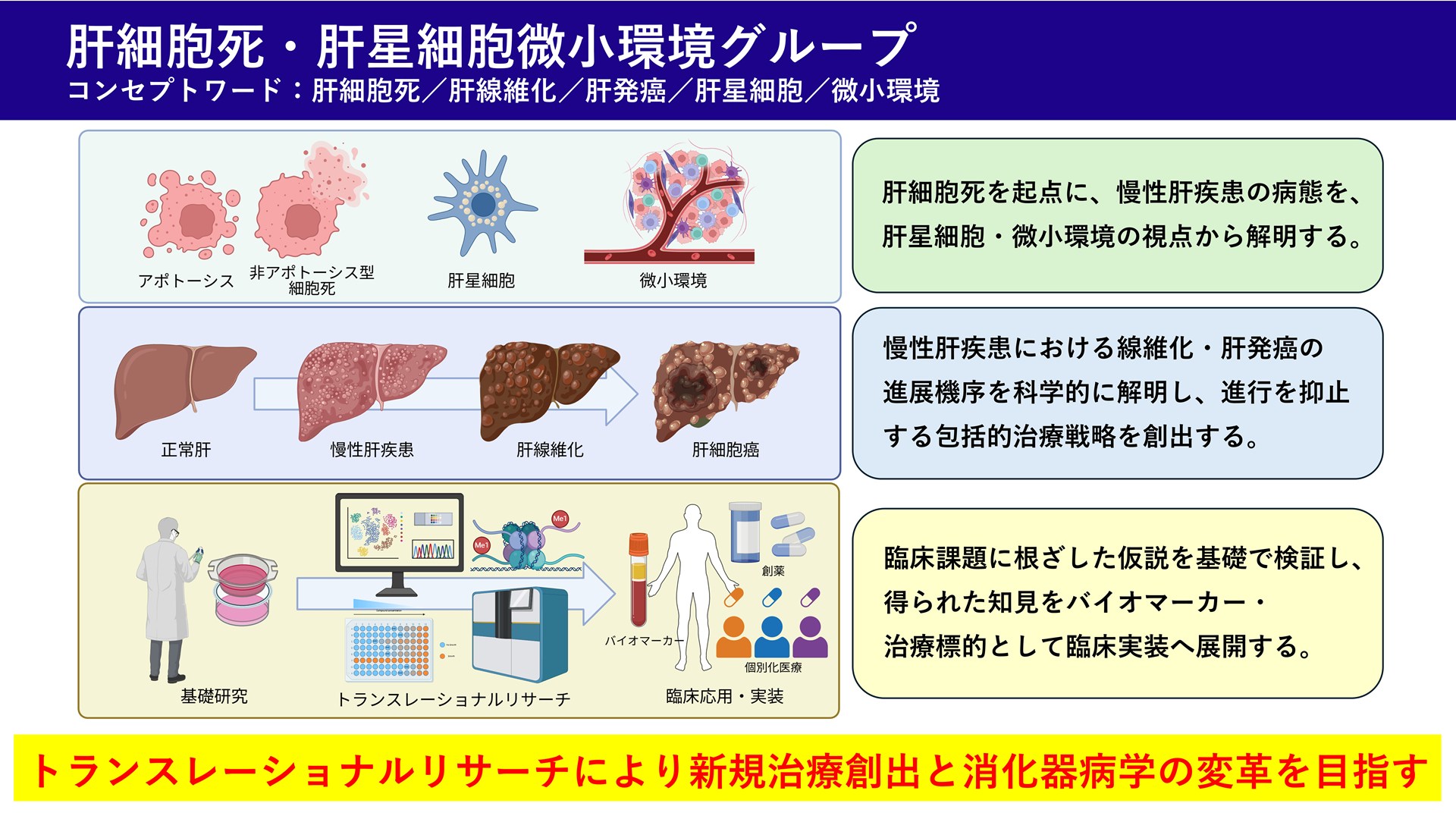
肝細胞死を起点とする慢性肝疾患の病態進展機序の解明
肝細胞死のタイプ(アポトーシス/非アポトーシス型細胞死)が慢性肝疾患の病態をどのように規定し、線維化・発癌の進展に寄与するかを解析します。細胞死に伴うDAMPs放出を起点として活性化される受容体シグナル、サイトカイン/ケモカイン回路、免疫細胞(マクロファージ、好中球、T細胞等)の時空間ダイナミクスを、当グループが構築してきた肝細胞死誘導モデル(in vivo/in vitro)で系統的に検証し、病態進展の因果機序を明らかにします。さらに得られた知見を臨床検体(生検・切除組織・血液)で検証し、進展予測バイオマーカーの同定と、治療標的候補の創出を目指す。
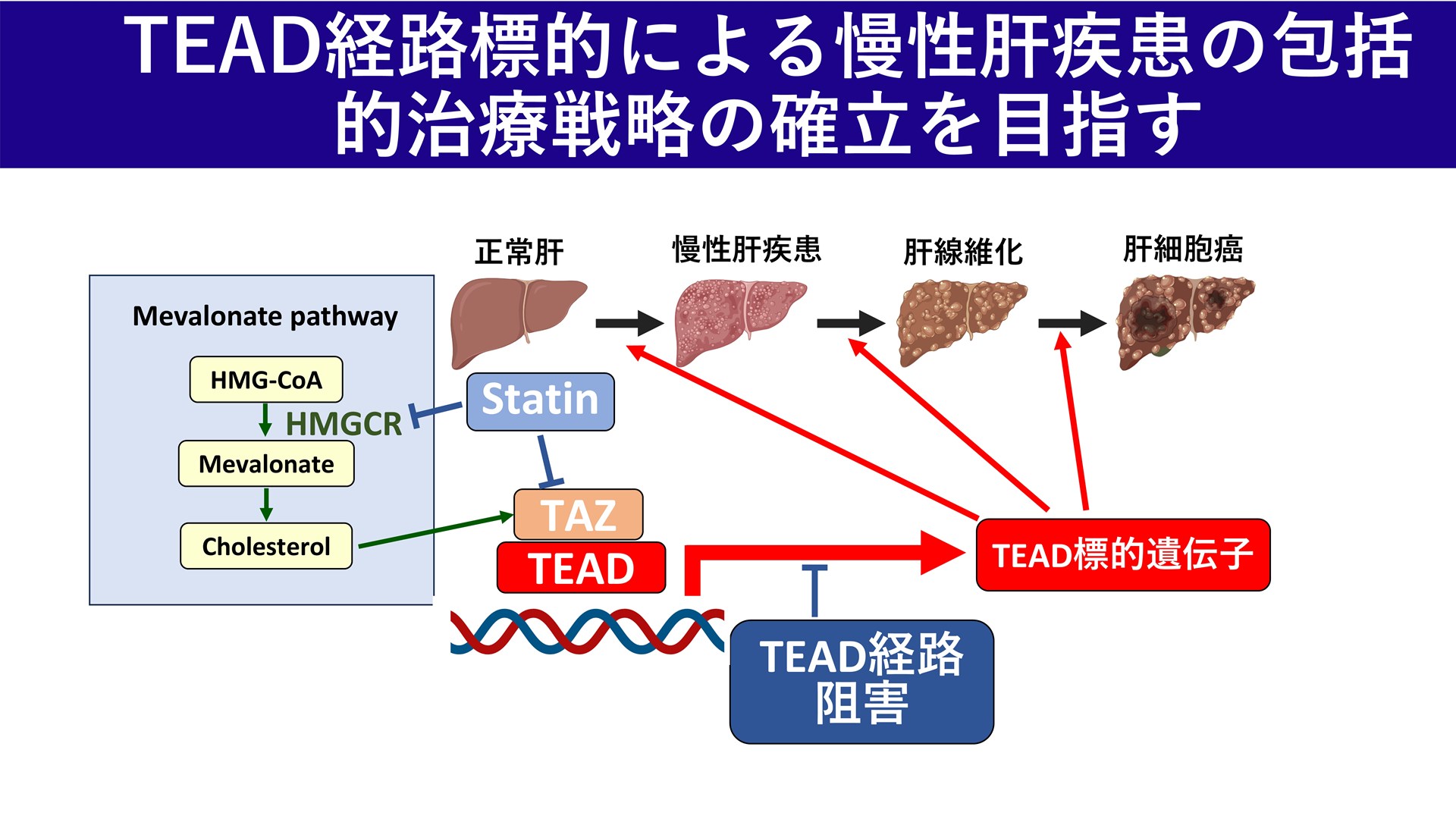
慢性肝疾患における肝線維化・肝細胞癌の進展の包括的治療戦略の確立
慢性肝疾患は、肝細胞死などに引き続く炎症・免疫応答と肝星細胞活性化を介して線維化が進展し、最終的に肝細胞癌の発症へと連なる連続的病態です。一方、現行の治療は線維化あるいは肝細胞癌のいずれかを個別に標的とする介入が中心で、病態の連続性を統合して制御する治療体系は十分に確立されていません。そこで本研究では、背景肝の炎症・線維化制御と、発癌・再発リスク低減を同一の枠組みで達成する包括的治療戦略の確立を目指します。病態ドライバーの同定と介入検証を通じて、予防・早期介入型の新規治療コンセプトの確立を目指す。
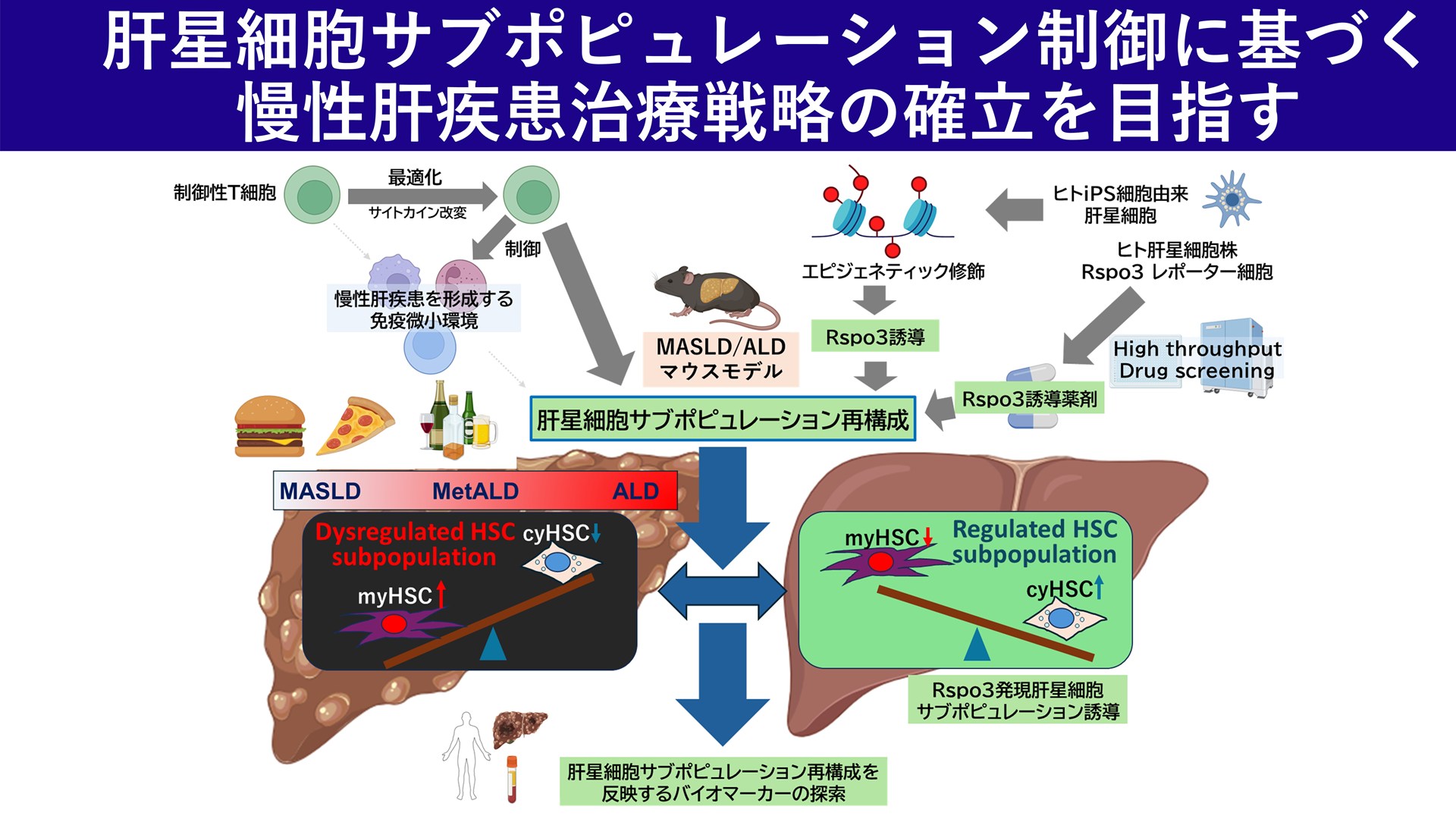
肝星細胞サブポピュレーションに着目した微小環境制御による慢性肝疾患の治療戦略の確立
肝星細胞は活性化により線維化や肝発癌を促進することが知られていますが、近年、我々は肝星細胞が多様なサブポピュレーションから成り、その構成比の不均衡が病態進展や予後と関連することを明らかにした。本研究では、肝星細胞の可塑性と集団動態に着目し、線維化・発癌を駆動するサブポピュレーションと細胞間相互作用を同定します。単一細胞解析・空間解析(single-cell RNA-seq/spatial transcriptomics)により肝星細胞の状態遷移と局在を可視化し、免疫細胞・胆管細胞・血管内皮とのシグナルネットワークを明らかにします。候補因子はクロマチンアクセシビリティ・エンハンサー解析に加え、共培養・オルガノイドで機能検証します。さらに細胞外基質産生、免疫調節、腫瘍ニッチ形成への寄与を定量化し、標的化可能な機序を同定し、治療戦略の確立を目指す。
将来展望:病態連鎖の可視化と層別化に基づく個別化医療の実装
今後は、肝細胞死を起点とする炎症・免疫応答、肝星細胞(HSC)を中心とした微小環境の再構築、線維化の進展、そして肝発癌へと至る一連の「病態連鎖」を、時間軸(いつ起きるか)と空間軸(どこで起きるか)の両面から定量化し、病期が次の段階へ移行する分岐点を特定します。分岐点とは、例えば転写制御ネットワークの切り替えや、細胞間シグナル(サイトカイン、増殖因子、細胞外基質、免疫チェックポイントなど)の再配線が生じる局面であり、ここを同定することが予防・早期介入の鍵になります。 そのために、臨床検体(生検・切除組織・血液)を用いた多層オミクス解析(single-cell/spatial解析、クロマチン解析、プロテオミクス等)を統合し、病態の地図(多層オミクス・アトラス)を構築します。得られた情報は研究用に留めず、再現性と汎用性を担保した指標として、現場で測定可能な検査系(血中バイオマーカー、組織スコア、画像・デジタル病理指標など)へ落とし込みます。 さらに、同定した病態ドライバーや分岐点を標的として、抗線維化・抗発癌の予防/早期介入型治療を開発します。バイオマーカーにより患者を層別化し、「誰に、いつ、どの介入が効くか」を検証可能な臨床研究へ展開するとともに、産学連携による診断法・治療法の社会実装を推進します。最終的には、慢性肝疾患の進展と再発を抑止する新しい診療モデルを確立し、診断と治療のTransformationに資することを目指します。
【主要論文】
- Kudo S, Hikita H, Saito Y, Murai K, Kodama T, Tatsumi T, Takehara T. Collaborative orchestration of BH3-only proteins governs Bak/Bax-dependent hepatocyte apoptosis under antiapoptotic protein-deficiency in mice. Cell Death Differ. 2025 Jun;32(6):1153-1166.
- Sugimoto A, Saito Y, Wang G, Sun Q, Yin C, Lee KH, Geng Y, Rajbhandari P, Hernandez C, Steffani M, Qie J, Savage T, Goyal DM, Ray KC, Neelakantan TV, Yin D, Melms J, Lehrich BM, Yasaka TM, Liu S, Oertel M, Lan T, Guillot A, Peiseler M, Filliol A, Kanzaki H, Fujiwara N, Ravi S, Izar B, Brosch M, Hampe J, Remotti H, Argemi J, Sun Z, Kendall TJ, Hoshida Y, Tacke F, Fallowfield JA, Blockley-Powell SK, Haeusler RA, Steinman JB, Pajvani UB, Monga SP, Bataller R, Masoodi M, Arpaia N, Lee YA, Stockwell BR, Augustin HG, Schwabe RF. Hepatic stellate cells control liver zonation, size and functions via R-spondin 3. Nature. 2025 Apr;640(8059):752-761.
- Saito Y, Yin D, Kubota N, Wang X, Filliol A, Remotti H, Nair A, Fazlollahi L, Hoshida Y, Tabas I, Wangensteen KJ, Schwabe RF. A Therapeutically Targetable TAZ-TEAD2 Pathway Drives the Growth of Hepatocellular Carcinoma via ANLN and KIF23. Gastroenterology. 2023 Jun;164(7):1279-1292.
- Filliol A, Saito Y, Nair A, Dapito DH, Yu LX, Ravichandra A, Bhattacharjee S, Affo S, Fujiwara N, Su H, Sun Q, Savage TM, Wilson-Kanamori JR, Caviglia JM, Chin L, Chen D, Wang X, Caruso S, Kang JK, Amin AD, Wallace S, Dobie R, Yin D, Rodriguez-Fiallos OM, Yin C, Mehal A, Izar B, Friedman RA, Wells RG, Pajvani UB, Hoshida Y, Remotti HE, Arpaia N, Zucman-Rossi J, Karin M, Henderson NC, Tabas I, Schwabe RF. Opposing roles of hepatic stellate cell subpopulations in hepatocarcinogenesis. Nature. 2022 Oct;610(7931):356-365.
- Wang X, Zeldin S, Shi H, Zhu C, Saito Y, Corey KE, Osganian SA, Remotti HE, Verna EC, Pajvani UB, Schwabe RF, Tabas I. TAZ-induced Cybb contributes to liver tumor formation in non-alcoholic steatohepatitis. J Hepatol. 2022 Apr;76(4):910-920.
- Affo S, Nair A, Brundu F, Ravichandra A, Bhattacharjee S, Matsuda M, Chin L, Filliol A, Wen W, Song X, Decker A, Worley J, Caviglia JM, Yu L, Yin D, Saito Y, Savage T, Wells RG, Mack M, Zender L, Arpaia N, Remotti HE, Rabadan R, Sims P, Leblond AL, Weber A, Riener MO, Stockwell BR, Gaublomme J, Llovet JM, Kalluri R, Michalopoulos GK, Seki E, Sia D, Chen X, Califano A, Schwabe RF. Promotion of cholangiocarcinoma growth by diverse cancer-associated fibroblast subpopulations. Cancer Cell. 2021 Jun 14;39(6):866-882.e11.
- Mizutani N, Hikita H, Saito Y, Myojin Y, Sato K, Urabe M, Kurahashi T, Shiode Y, Sakane S, Murai K, Nozaki Y, Kodama T, Sakamori R, Yoshida Y, Tatsumi T, Takehara T. Gab1 in livers with persistent hepatocyte apoptosis has an antiapoptotic effect and reduces chronic liver injury, fibrosis, and tumorigenesis. Am J Physiol Gastrointest Liver Physiol. 2021 Jun 1;320(6):G958-G968.
- Nozaki Y, Hikita H, Tanaka S, Fukumoto K, Urabe M, Sato K, Myojin Y, Doi A, Murai K, Sakane S, Saito Y, Kodama T, Sakamori R, Tatsumi T, Takehara T. Persistent hepatocyte apoptosis promotes tumorigenesis from diethylnitrosamine-transformed hepatocytes through increased oxidative stress, independent of compensatory liver regeneration. Sci Rep. 2021 Feb 9;11(1):3363.
- Saito Y, Hikita H, Nozaki Y, Kai Y, Makino Y, Nakabori T, Tanaka S, Yamada R, Shigekawa M, Kodama T, Sakamori R, Tatsumi T, Takehara T. DNase II activated by the mitochondrial apoptotic pathway regulates RIP1-dependent non-apoptotic hepatocyte death via the TLR9/IFN-β signaling pathway. Cell Death Differ. 2019 Mar;26(3):470-486.
- Tanaka S, Hikita H, Tatsumi T, Sakamori R, Nozaki Y, Sakane S, Shiode Y, Nakabori T, Saito Y, Hiramatsu N, Tabata K, Kawabata T, Hamasaki M, Eguchi H, Nagano H, Yoshimori T, Takehara T. Rubicon inhibits autophagy and accelerates hepatocyte apoptosis and lipid accumulation in nonalcoholic fatty liver disease in mice. Hepatology. 2016 Dec;64(6):1994-2014.
- Hikita H, Kodama T, Tanaka S, Saito Y, Nozaki Y, Nakabori T, Shimizu S, Hayashi Y, Li W, Shigekawa M, Sakamori R, Miyagi T, Hiramatsu N, Tatsumi T, Takehara T. Activation of the Mitochondrial Apoptotic Pathway Produces Reactive Oxygen Species and Oxidative Damage in Hepatocytes That Contribute to Liver Tumorigenesis. Cancer Prev Res (Phila). 2015 Aug;8(8):693-701.
- Kodama T, Hikita H, Kawaguchi T, Saito Y, Tanaka S, Shigekawa M, Shimizu S, Li W, Miyagi T, Kanto T, Hiramatsu N, Tatsumi T, Takehara T. The Bcl-2 homology domain 3 (BH3)-only proteins Bim and bid are functionally active and restrained by anti-apoptotic Bcl-2 family proteins in healthy liver. J Biol Chem. 2013 Oct 18;288(42):30009-30018.
- Hikita H, Kodama T, Shimizu S, Li W, Shigekawa M, Tanaka S, Hosui A, Miyagi T, Tatsumi T, Kanto T, Hiramatsu N, Morii E, Hayashi N, Takehara T. Bak deficiency inhibits liver carcinogenesis: a causal link between apoptosis and carcinogenesis. J Hepatol. 2012 Jul;57(1):92-100.
- Hikita H, Takehara T, Kodama T, Shimizu S, Shigekawa M, Hosui A, Miyagi T, Tatsumi T, Ishida H, Li W, Kanto T, Hiramatsu N, Shimizu S, Tsujimoto Y, Hayashi N. Delayed-onset caspase-dependent massive hepatocyte apoptosis upon Fas activation in Bak/Bax-deficient mice. Hepatology. 2011 Jul;54(1):240-51.
- Hikita H, Takehara T, Shimizu S, Kodama T, Shigekawa M, Iwase K, Hosui A, Miyagi T, Tatsumi T, Ishida H, Li W, Kanto T, Hiramatsu N, Hayashi N. The Bcl-xL inhibitor, ABT-737, efficiently induces apoptosis and suppresses growth of hepatoma cells in combination with sorafenib. Hepatology. 2010 Oct;52(4):1310-21.
- Shimizu S, Takehara T, Hikita H, Kodama T, Miyagi T, Hosui A, Tatsumi T, Ishida H, Noda T, Nagano H, Doki Y, Mori M, Hayashi N. The let-7 family of microRNAs inhibits Bcl-xL expression and potentiates sorafenib-induced apoptosis in human hepatocellular carcinoma. J Hepatol. 2010 May;52(5):698-704.
- Hikita H, Takehara T, Kodama T, Shimizu S, Hosui A, Miyagi T, Tatsumi T, Ishida H, Ohkawa K, Li W, Kanto T, Hiramatsu N, Hennighausen L, Yin XM, Hayashi N. BH3-only protein bid participates in the Bcl-2 network in healthy liver cells. Hepatology. 2009 Dec;50(6):1972-80.
- Hikita H, Takehara T, Shimizu S, Kodama T, Li W, Miyagi T, Hosui A, Ishida H, Ohkawa K, Kanto T, Hiramatsu N, Yin XM, Hennighausen L, Tatsumi T, Hayashi N. Mcl-1 and Bcl-xL cooperatively maintain integrity of hepatocytes in developing and adult murine liver. Hepatology. 2009 Oct;50(4):1217-26.
- Takehara T, Tatsumi T, Suzuki T, Rucker EB 3rd, Hennighausen L, Jinushi M, Miyagi T, Kanazawa Y, Hayashi N. Hepatocyte-specific disruption of Bcl-xL leads to continuous hepatocyte apoptosis and liver fibrotic responses. Gastroenterology. 2004 Oct;127(4):1189-97.
