膵・肝病態インターセプションリサーチグループ
グループリーダー:牧野祐紀
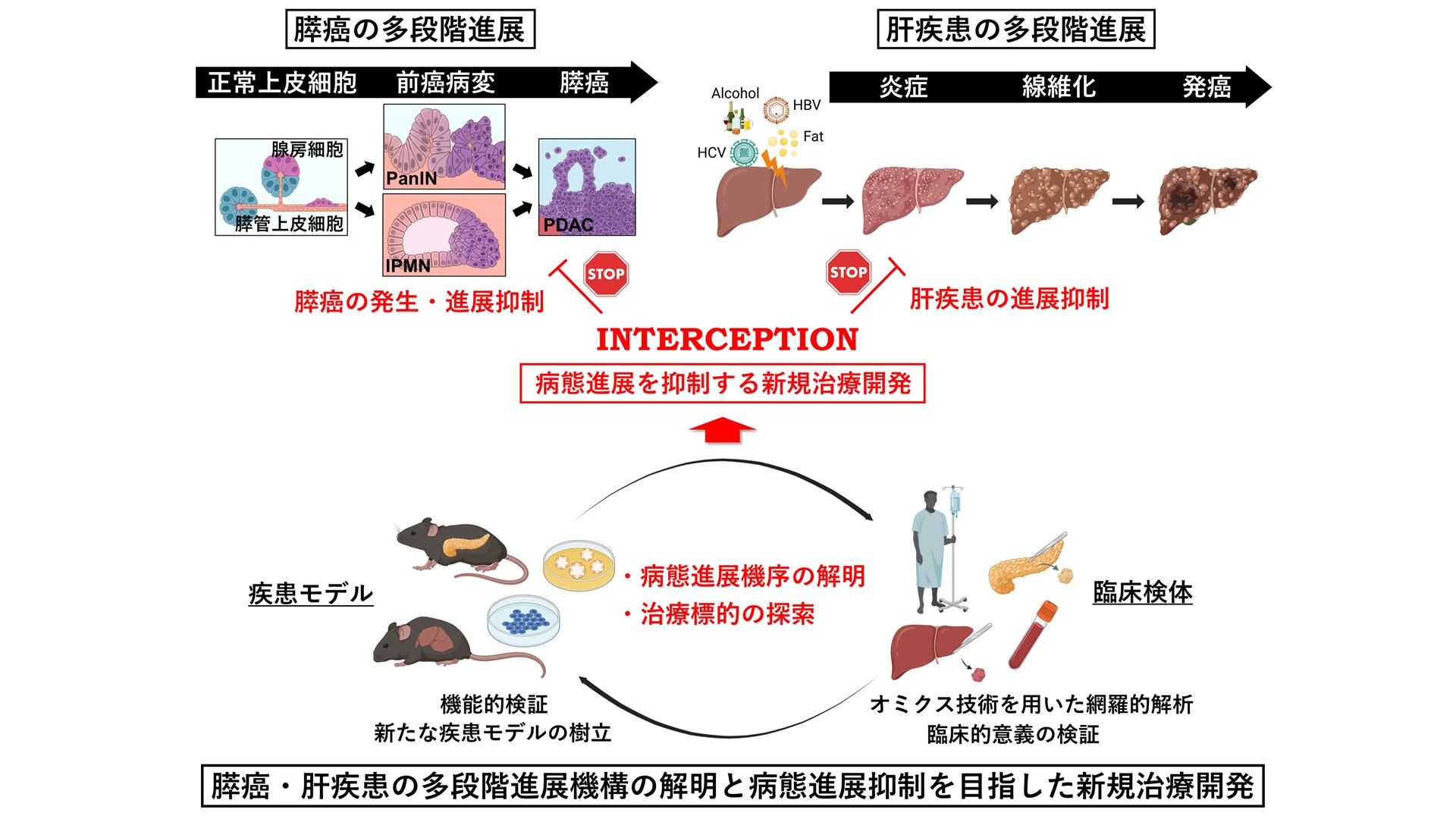
コンセプト:膵臓と肝臓の多段階病態進展機序の解明
膵臓の発癌、肝臓に生じる炎症、線維化、発癌といった現象の病態解明と治療開発を目的とした基礎研究を行っています。どちらの臓器も生命に関わる重要な疾患が多いですが、いずれも多くの場合は段階的な病態の変化を経て進展していきます。私たちは、それぞれの疾患が進展する過程において、最初の変化が生じるのは何故なのか、どのようなメカニズムで次の段階に進むのかを明らかにすることを目標に、各段階で生じる分子の変化、種々の細胞の働きの変化について解析しています。こうした変化を解明することで、特定の分子や細胞を標的にした治療開発に繋げ、病態の進展を“インターセプト”することが目標です。膵臓、肝臓において、有効な分子標的治療が開発されているのは一部の疾患に限られ、多くの疾患では非特異的な治療法や対症療法に依存しているのが現状です。私たちは、未だ有効な治療の乏しい疾患・病態に対し、独自の視点から新たな治療法を開発することで、既存の診療の概念転換することを目指します。
オミクス解析で解き明かす膵癌発生・進展・治療抵抗性メカニズム
膵癌は早期発見が難しい上、ひとたび発症すると非常に予後の悪い最大の難治癌です。一方、膵癌といえども早期に診断し治療できれば十分に根治が望めます。膵癌は正常の上皮細胞がいきなり癌細胞に変化して発生するのではなく、多くの場合には膵上皮内腫瘍性病変(PanIN)や膵管内乳頭粘液性腫瘍(IPMN)とよばれる前癌病変を経て発生します。前癌病変が癌に進展し、さらに転移能を獲得するには年単位の時間を要すると考えられており、前癌病変のうちに早期発見・早期治療介入を行う機会があります。私たちは、胆膵 Onco-Endoscopyグループとの連携のもとオミクス技術による臨床検体の網羅的解析に基づき膵癌の発癌・進展過程および治療に伴う細胞の特性の変化、微小環境の変化を解析し、独自の疾患モデルを用いてその意義を検証します。これらの知見を膵癌の早期発見や膵癌の発生・進展を食い止める方法の開発に繋げ、増加の一途を辿る膵癌死亡を少しでも減らすことを目指しています。
IPMNを標的とした膵癌予防の実現
膵臓の前癌病変のうち、PanIN は顕微鏡でしか観察できない微小病変である一方、IPMNは嚢胞性腫瘍であり、超音波検査などの簡単な画像検査で前癌段階から発見できるという特徴があります。IPMNは非常に頻度の高い疾患ですが、IPMNがある人はない人に比べて膵癌のリスクが何倍にも上昇します。そのためIPMNは前癌段階から治療介入の対象となり得る病変ですが、現時点では外科的切除以外に有効な治療法がありません。その背景には、IPMNの病態メカニズムが十分に解明されていないという課題があります。私たちはこれまでIPMNの疾患モデルの確立を行ってきたほか、臨床検体を用いた解析によりIPMNの発生・進展に関連する分子機構や免疫微小環境の変化の一端を明らかにしてきました。これらの知見をさらに発展・深化させ、IPMNに対する正確な悪性リスク評価と新規治療開発を実現し、膵癌に対する予防的治療法の確立に繋げます。
がん抑制遺伝子p53の“働き過ぎ”を起点とした肝病態機構の解析
p53は“ゲノムの守護神”と称される最も有名ながん抑制遺伝子であり、その機能喪失は肝臓を含む全身の様々な癌の発生に関与しています。一方、肝疾患を伴う肝臓ではウイルス、アルコール、自己免疫など種々の原因によるストレス刺激によってp53が過剰に働いています。私たちは以前よりその役割について研究しており、肝細胞でp53が過剰に働くと、それだけで肝臓の炎症・線維化・発癌が生じることを見出しました。すなわち、従来がん抑制遺伝子として知られてきたp53が肝病態進展のマスター・レギュレーターとして働くことが分かりました。現在、p53がどのようにして肝臓の炎症・線維化・発癌を誘導するのかさらに研究を進めています。そのメカニズムの中から、肝疾患の進展を止めるための治療標的を探索します。
類洞内皮細胞に着目した肝疾患の病態解明
類洞内皮細胞は肝臓独特の毛細血管網である類洞を構成する特殊な内皮細胞で、通常の毛細血管内皮細胞と異なる働きをもっており、様々な肝疾患においてその働きが変化することが知られています。特に先天性心疾患に対するFontan術後肝合併症(Fontan-associatedliverdisease;FALD)は特殊な血行動態に起因して生じる慢性的・進行性の肝障害であり、その病態は類洞内皮細胞の働きと密接に関わることが想定されます。近年Fontan術後患者の生命予後改善に伴いFALDが顕在化することが多く、重要な合併症として注目されていますが、未だ有効な治療法や疾患バイオマーカーが開発されていません。私たちは類洞内皮細胞の働きという観点から、FALDを含めたさまざまな肝疾患の病態制御分子を解明し、新規治療開発に繋げたいと考えています。
将来展望:膵癌と肝疾患の診療パラダイムシフト
膵癌診療において既存の「診断」「治療」に加えた「予防的治療」という概念を導入し、膵癌を予防可能な疾患にすること、また十分な治療法の存在しない肝疾患領域に、新たな治療法を導入することを実現したいと思っています。
【主要論文】
- Quoc-Huy Trinh V, Ankenbauer KE, Torbit SM, Taranto CP, Liu J, Batardiere M, Kumar B, Maurer HC, Revetta F, Chen Z, Kruse ARS, Judd AM, Copeland C, Wong J, Ben-Levy O, Jarvis B, Brown M, Brown JW, Das K, Makino Y, Spraggins JM, Lau KS, Azadi P, Maitra A, Tan MCB, DelGiorno KE. Mutant GNAS drives a pyloric metaplasia with tumor suppressive glycans in intraductal papillary mucinous neoplasia. Cell Rep. 2025 Dec 23;44(12):116684.
- Makino Y, Oyama K, Sagara A, Thege FI, Maitra A. Molecular pathology of intraductal papillary mucinous neoplasms of the pancreas: current understanding and perspectives on malignant progression. J Gastroenterol. 2025 Nov 26. doi: 10.1007/s00535-025-02328-7. Epub ahead of print. PMID: 41296011.
- Chen Y, Ballarò R, Sans M, Thege FI, Zuo M, Dou R, Min J, Yip-Schneider M, Zhang J, Wu R, Irajizad E, Makino Y, Rajapakshe KI, Rudsari HK, Hurd MW, León-Letelier RA, Katayama H, Ostrin E, Vykoukal J, Dennison JB, Do KA, Hanash SM, Wolff RA, Guerrero PA, Kim M, Schmidt CM, Maitra A, Fahrmann JF. Long-chain sulfatide enrichment is an actionable metabolic vulnerability in intraductal papillary mucinous neoplasm (IPMN)-associated pancreatic cancers. Gut. 2025 Sep 8;74(10):1638-1652.
- Makino Y, Rajapakshe KI, Chellakkan Selvanesan B, Okumura T, Date K, Dutta P, Abou-Elkacem L, Sagara A, Min J, Sans M, Yee N, Siemann MJ, Enriquez J, Smith P, Bhattacharya P, Kim M, Dede M, Hart T, Maitra A, Thege FI. Metabolic reprogramming by mutant GNAS creates an actionable dependency in intraductal papillary mucinous neoplasms of the pancreas. Gut. 2024 Dec 10;74(1):75-88.
- Semaan A, Bernard V, Wong J, Makino Y, Swartzlander DB, Rajapakshe KI, Lee JJ, Officer A, Schmidt CM, Wu HH, Scaife CL, Affolter KE, Nachmanson D, Firpo MA, Yip-Schneider M, Lowy AM, Harismendy O, Sen S, Maitra A, Jakubek YA, Guerrero PA. Integrated Molecular Characterization of Intraductal Papillary Mucinous Neoplasms: An NCI Cancer Moonshot Precancer Atlas Pilot Project. Cancer Res Commun. 2023 Oct 10;3(10):2062-2073.
- Sans M, Makino Y, Min J, Rajapakshe KI, Yip-Schneider M, Schmidt CM, Hurd MW, Burks JK, Gomez JA, Thege FI, Fahrmann JF, Wolff RA, Kim MP, Guerrero PA, Maitra A. Spatial Transcriptomics of Intraductal Papillary Mucinous Neoplasms of the Pancreas Identifies NKX6-2 as a Driver of Gastric Differentiation and Indolent Biological Potential. Cancer Discov. 2023 Aug 4;13(8):1844-1861.
- Makino Y, Hikita H, Kato S, Sugiyama M, Shigekawa M, Sakamoto T, Sasaki Y, Murai K, Sakane S, Kodama T, Sakamori R, Kobayashi S, Eguchi H, Takemura N, Kokudo N, Yokoi H, Mukoyama M, Tatsumi T, Takehara T. STAT3 is Activated by CTGF-mediated Tumor-stroma Cross Talk to Promote HCC Progression. Cell Mol Gastroenterol Hepatol. 2023;15(1):99-119.
- Makino Y, Hikita H, Fukumoto K, Sung JH, Sakano Y, Murai K, Sakane S, Kodama T, Sakamori R, Kondo J, Kobayashi S, Tatsumi T, Takehara T. Constitutive Activation of the Tumor Suppressor p53 in Hepatocytes Paradoxically Promotes Non-Cell Autonomous Liver Carcinogenesis. Cancer Res. 2022 Aug 16;82(16):2860-2873.
- Urabe M, Hikita H, Saito Y, Kudo S, Fukumoto K, Mizutani N, Myojin Y, Doi A, Sato K, Sakane S, Makino Y, Kodama T, Sakamori R, Tatsumi T, Takehara T. Activation of p53 After Irradiation Impairs the Regenerative Capacity of the Mouse Liver. Hepatol Commun. 2022 Feb;6(2):411-422.
- Makino Y, Hikita H, Kodama T, Shigekawa M, Yamada R, Sakamori R, Eguchi H, Morii E, Yokoi H, Mukoyama M, Hiroshi S, Tatsumi T, Takehara T. CTGF Mediates Tumor-Stroma Interactions between Hepatoma Cells and Hepatic Stellate Cells to Accelerate HCC Progression. Cancer Res. 2018 Sep 1;78(17):4902-4914.
- Kodama T, Takehara T, Hikita H, Shimizu S, Shigekawa M, Tsunematsu H, Li W, Miyagi T, Hosui A, Tatsumi T, Ishida H, Kanto T, Hiramatsu N, Kubota S, Takigawa M, Tomimaru Y, Tomokuni A, Nagano H, Doki Y, Mori M, Hayashi N. Increases in p53 expression induce CTGF synthesis by mouse and human hepatocytes and result in liver fibrosis in mice. J Clin Invest. 2011 Aug;121(8):3343-56.
