B型肝炎ウイルス(HBV)研究グループ
グループリーダー:村井一裕
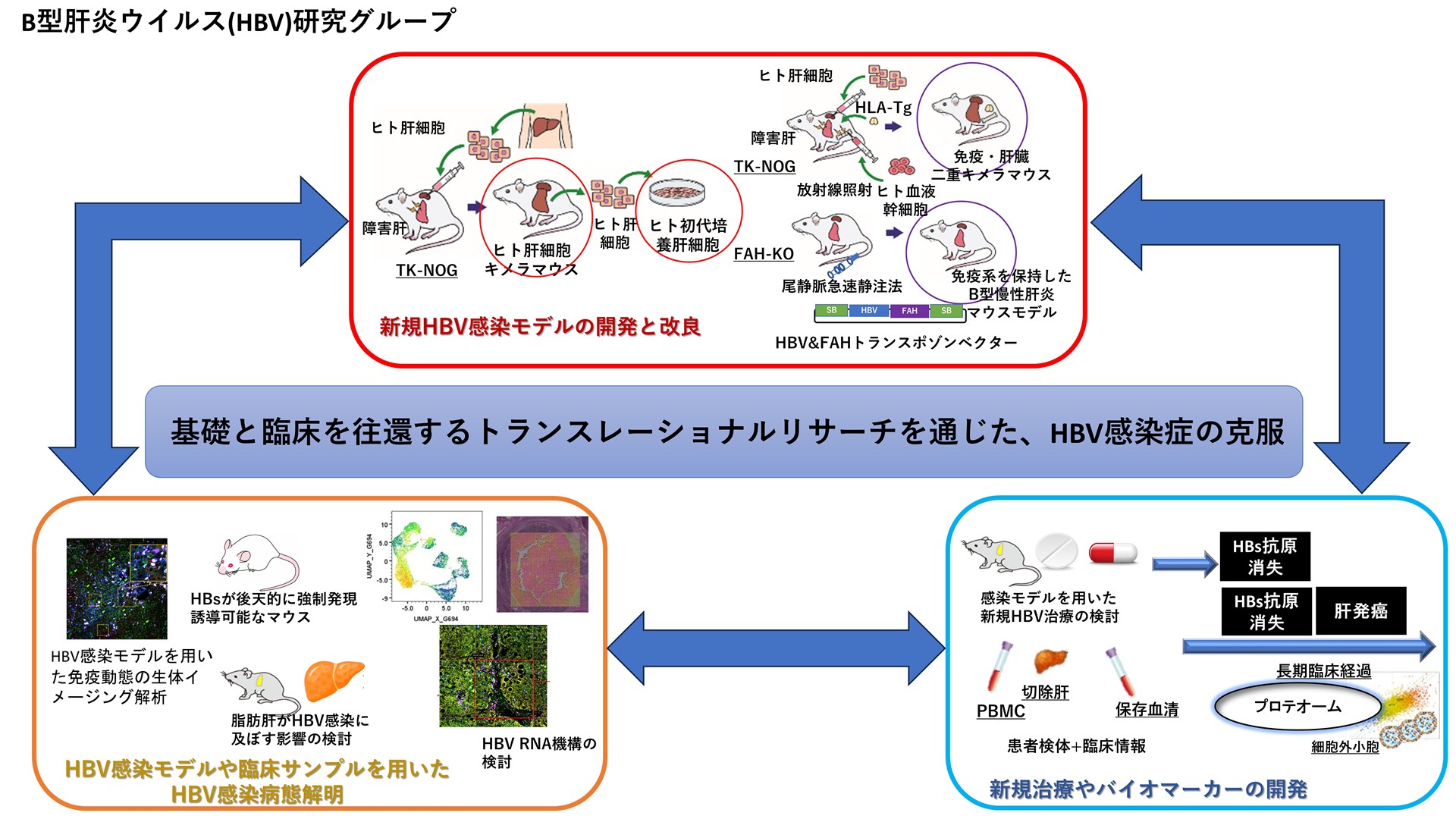
コンセプト:HBVの完全排除を目指す
B型肝炎ウイルス(HBV)は世界に約2億5千万人の感染者が存在し、慢性持続感染は肝炎・肝硬変・肝細胞癌(HCC)へと進展します。核酸アナログ製剤(NUC)によりHBV複製の強力な抑制は可能となりましたが、感染肝細胞核内に形成されるcovalently closed circular DNA(cccDNA)や宿主ゲノムに組み込まれたHBVゲノムの存在により、治療中止後の再燃や発癌リスクは依然として残存し、ウイルスの完全排除には至っていません。 当グループは、B型慢性肝炎患者を対象とした長期観察研究による臨床経過解析に加え、細胞およびマウスを用いた感染モデル、ならびに臨床検体を活用した宿主・ウイルス遺伝子相互作用解析を統合的に行い、HBV持続感染および発癌に関与する分子機構の解明を進めています。これらの成果を基盤として、cccDNA、組込みHBVを標的とした治療やHBVの機能的治癒あるいは完全排除を高率に達成できる治療の確立と、治療効果や予後を予測可能なバイオマーカーの開発を推進し、HBV感染症の克服を目指します。
B型慢性肝炎患者における発癌リスク・新規病態進展予測バイオマーカーの同定
臨床研究では、多施設大規模コホートを用いた長期追跡解析により、NUC投与下のB型慢性肝炎患者において、非肝硬変例であっても、治療開始後10年以上経過した後も年率約1%で肝細胞癌(HCC)発症リスクが持続することを明らかにしました(2)。この結果は、NUC治療によっても発癌リスクが完全には消失しないことを示しており、長期的な発癌サーベイランスの重要性を示唆します。さらに、新規バイオマーカー候補であるGDF15がHCC発症を高精度に予測し得ることを見出し、従来指標を補完する新たなリスク層別化ツールとなる可能性を示しました(4)。これらの成果は、個別化医療に基づく発癌予測およびサーベイランス戦略の構築につながると期待されます。
HBV感染時の免疫応答・自然免疫変動
HBV感染下では、ウイルス特異的免疫応答の低下や免疫担当細胞の機能変化が生じ、これらがウイルス持続感染の成立に深く関与します。当グループは、HBV慢性感染マウスモデルにおいて、ウイルス特異的CD8⁺T細胞が疲弊表現型を示し、その頻度が増加していることを明らかにしてきました(3)。さらに、これら疲弊T細胞の表現型や機能が血清HBs抗原量やHBV DNAと関連することを示し、免疫状態が病態形成に密接に関与することを示唆しました。 また、C型肝炎ウイルス(HCV)との共感染時には、HCV感染により誘導されるRIG-I like helicase経路を介した細胞内自然免疫応答が活性化され、ヒト肝細胞においてHBV複製が抑制されることを示しました(10)。これらの知見は、T細胞機能回復や自然免疫賦活を標的とした免疫制御型治療の有効性を支持するものであり、機能的治癒を目指した新規治療法開発につながると期待されます。
HBV関連肝癌の脆弱性因子
HBV関連肝細胞癌(HCC)においては、ウイルス感染を背景とした特異的な分子異常が腫瘍の発生・進展に関与すると考えられています。当グループは、HBV関連HCCにおいて腫瘍細胞の生存や増殖を支える分子であるINSIG2の抑制により腫瘍細胞の増殖能が低下し細胞増殖が抑制されることを明らかにしました。さらに、INSIG2が細胞周期に関連するシグナル経路を介して腫瘍維持に寄与する可能性を示し、HBV関連HCCにおける治療標的となり得る脆弱性因子であることを見出しました(5)。これらの分子を標的とすることで、従来治療とは異なる作用機序に基づくHBV関連肝癌に特異的な治療戦略の構築が可能となり、難治症例に対する新たな治療選択肢の創出につながると期待されます。
新規治療の開発
新規治療法の開発として、当グループはHBV持続感染の根幹であるcccDNAを標的としたCRISPR/Cas9遺伝子編集治療に取り組み、ヒト肝細胞を用いた感染モデルにおいてcccDNA量の低下およびHBV複製抑制が可能であることを示しました(7)。さらに、カプシド合成阻害薬とインターフェロン(IFN)を併用することで、細胞内自然免疫応答が相乗的に増強され、HBV複製およびウイルス抗原産生が強力に抑制されることを明らかにしました(8)。加えて、HBs抗原の分泌を阻害するFDA化合物をライブラリースクリーニングにより同定しました(1)。これら複数のアプローチを組み合わせることで、ウイルス増殖抑制にとどまらず、機能的治癒や完全排除を目指した多面的治療戦略の確立が期待されます。
将来展望:基礎と臨床を往還するトランスレーショナルリサーチを通じた、HBV感染症の克服
最終的には、HBVの持続感染を支える分子機構および免疫制御機構を標的とした新規治療戦略を確立し、HBVの完全排除ならびに肝発癌の抑止を実現することを目標としています。基礎と臨床を往還するトランスレーショナルリサーチを通じて、HBV感染症の克服に挑み続けます。
【主要論文】
- Shimoda A, Murai K, Hikita H, Minami S, Miyake T, Kuriki S, Sometani E, Sung J, Shigeno S, Higuchi Y, Maesaka K, Shirai K, Tahata Y, Saito Y, Kodama T, Takahashi T, Suemizu H, Takehara T. Auranofin, identified by FDA-approved drug library screening, inhibits HBs antigen secretion via lysosomal damage. PLoS One. 2026 Jan 16;21(1):e0340023.
- Murai K, Hikita H, Yamada R, Nishimura Y, Miyazaki M, Ishida H, Hosui A, Sakamori R, Tatsumi N, Ohkawa K, Doi Y, Nawa T, Egawa S, Yoshida Y, Nozaki Y, Imanaka K, Nakahara M, Sakakibara M, Yakushijin T, Ogawa H, Usui T, Matsumoto K, Oze T, Kuriki S, Sometani E, Sung J, Shimoda A, Shigeno S, Maesaka K, Shirai K, Doi A, Tahata Y, Saito Y, Kodama T, Tatsumi T, Yamada T, Takehara T. The Risk of Developing Hepatocellular Carcinoma Persists in Chronic Hepatitis B Patients Even After the Long-Term Administration of Nucleos(t)ide Analogs. Hepatol Res. 2025 Sep;55(9):1228-1238.
- Shigeno S, Kodama T, Murai K, Motooka D, Fukushima A, Nishio A, Hikita H, Tatsumi T, Okamoto T, Kanto T, Takehara T. Intrahepatic Exhausted Antiviral Immunity in an Immunocompetent Mouse Model of Chronic Hepatitis B. Cell Mol Gastroenterol Hepatol. 2025;19(1):101412.
- Sometani E, Hikita H, Murai K, Toyoda H, Tanaka S, Oze T, Sung J, Shimoda A, Fukuoka M, Shigeno S, Fukutomi K, Shirai K, Tahata Y, Saito Y, Nishio A, Furuta K, Kodama T, Sakamori R, Tatsumi T, Mita E, Umezawa A, Tanaka Y, Takehara T. High serum growth differentiation factor 15 is a risk factor for the occurrence of hepatocellular carcinoma in chronic hepatitis B patients treated with nucleos(t)ide analogs. Hepatol Res. 2025;55(1):22-33.
- Fukuoka M, Kodama T, Murai K, Hikita H, Sometani E, Sung J, Shimoda A, Shigeno S, Motooka D, Nishio A, Furuta K, Tatsumi T, Yusa K, Takehara T. Genome-wide loss-of-function genetic screen identifies INSIG2 as the vulnerability of hepatitis B virus-integrated hepatoma cells. Cancer Sci. 2024 Mar;115(3):859-870.
- Murai K, Hikita H, Kodama T, Kaibori M, Nishimura Y, Tatsumi T, Yamada T, Kanto T, Mochida S, Takehara T. The impact of the COVID-19 pandemic on hepatocellular carcinoma diagnosis and treatment in Japan: A multicenter collaborative observational study. Hepatol Res. 2024 May;54(5):439-450.
- Murai K, Kodama T, Hikita H, Shimoda A, Fukuoka M, Fukutomi K, Shigeno S, Shiode Y, Motooka D, Higuchi Y, Miyakawa K, Suemizu H, Ryo A, Tahata Y, Makino Y, Yamada R, Sakamori R, Tatsumi T, Takehara T. Inhibition of nonhomologous end joining-mediated DNA repair enhances anti-HBV CRISPR therapy. Hepatol Commun. 2022 Sep;6(9):2474-2487.
- Fukutomi K, Hikita H, Murai K, Nakabori T, Shimoda A, Fukuoka M, Yamai T, Higuchi Y, Miyakawa K, Suemizu H, Ryo A, Yamada R, Kodama T, Sakamori R, Tatsumi T, Takehara T. Capsid Allosteric Modulators Enhance the Innate Immune Response in Hepatitis B Virus-Infected Hepatocytes During Interferon Administration. Hepatol Commun. 2022 Feb;6(2):281-296.
- Yamai T, Hikita H, Fukuoka M, Fukutomi K, Murai K, Nakabori T, Yamada R, Miyakawa K, Watashi K, Ryo A, Kodama T, Sakamori R, Tatsumi T, Takehara T. SIRT1 enhances hepatitis virus B transcription independent of hepatic autophagy. Biochem Biophys Res Commun. 2020 Jun 18;527(1):64-70.
- Murai K, Hikita H, Kai Y, Kondo Y, Fukuoka M, Fukutomi K, Doi A, Yamai T, Nakabori T, Fukuda R, Takahashi T, Miyakawa K, Suemizu H, Ryo A, Yamada R, Kodama T, Sakamori R, Tatsumi T, Takehara T. Hepatitis C virus infection suppresses hepatitis B virus replication via the RIG-I-like helicase pathway. Sci Rep. 2020 Jan 22;10(1):941.
- Nakabori T, Hikita H, Murai K, Nozaki Y, Kai Y, Makino Y, Saito Y, Tanaka S, Wada H, Eguchi H, Takahashi T, Suemizu H, Sakamori R, Hiramatsu N, Tatsumi T, Takehara T. Sodium taurocholate cotransporting polypeptide inhibition efficiently blocks hepatitis B virus spread in mice with a humanized liver. Sci Rep. 2016 Jun 9;6:27782.
