SLD全身ネットワーク研究グループ
グループリーダー:坂根 貞嗣
コンセプト:全身性疾患 / 多臓器相関 / Borderless
SLDを「全身性疾患」の一つと捉え、多臓器連関の解明により、患者さんの生命予後を改善するための新規治療戦略を創出します。 MASLD(代謝機能障害関連脂肪性肝疾患)やALD(アルコール関連肝疾患)などの脂肪性肝疾患(SLD)を、心血管疾患や他臓器癌のリスクを伴う「全身性疾患」として再定義し、臓器や手法の垣根を越えて肝臓と全身臓器のネットワーク(多臓器相関)を解明します。臨床データ・基礎実験結果・AI解析を融合し、肝臓だけでなく全身を診る視点で、発症予防から予後改善までをトータルコーディネートする次世代のSLD診療体系構築の礎となるエビデンスの創出を目指します。
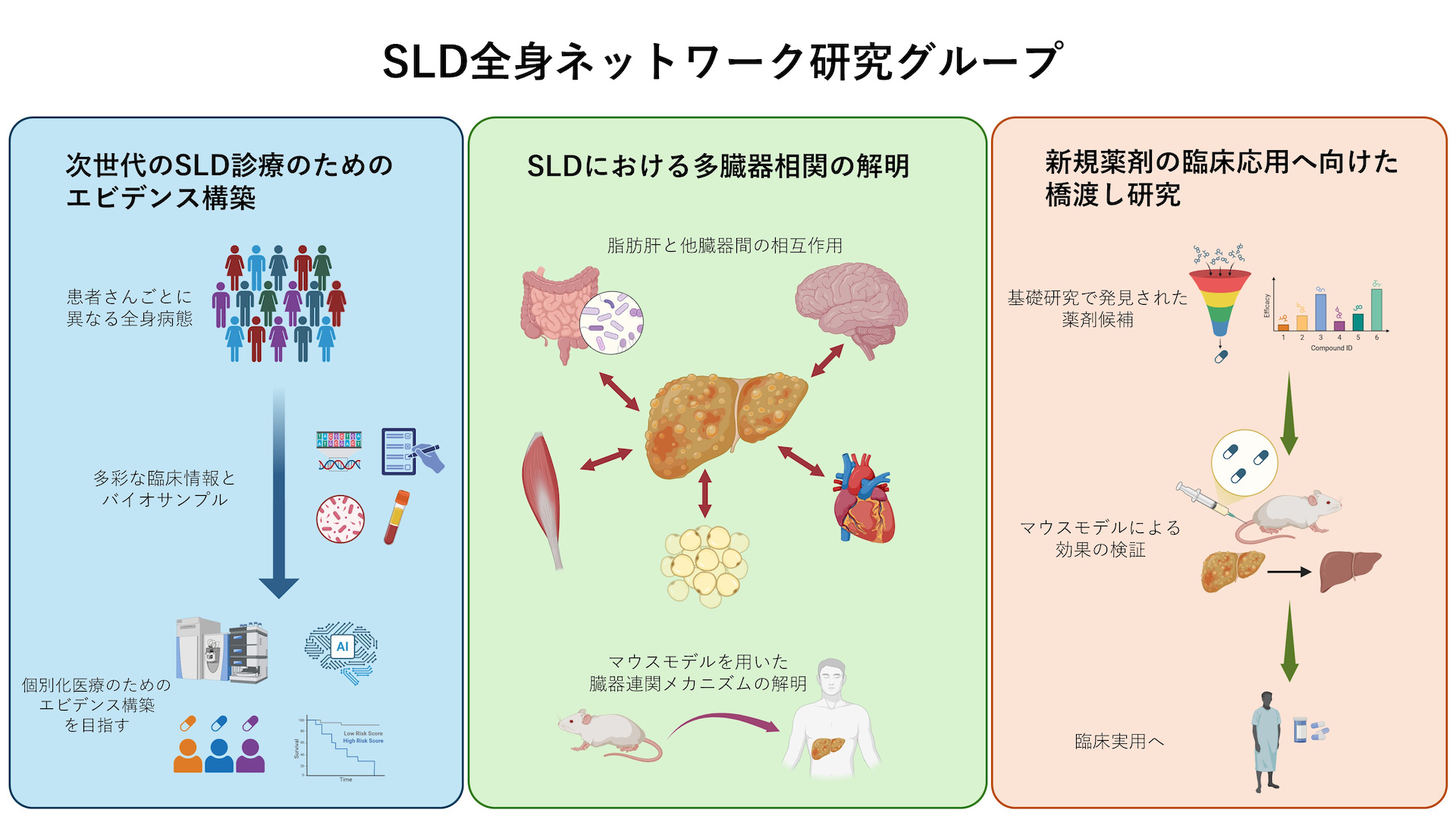
健康長寿の達成に向けたSLD精密医療のエビデンス構築
海外でのMASLD治療薬の実用化を筆頭に、SLD診療は今、大きな転換期を迎えています。しかし、SLDが全身性疾患である以上、肝臓局所の改善のみならず、患者さんの「健康長寿」を全人的に達成する新たな診療体系の構築が不可欠です。私たちは、多彩な臨床情報やバイオサンプルから得られるマルチモーダルなデータを統合的に解析し、精緻なエビデンスを蓄積していきます。これにより、非侵襲的な診断バイオマーカーの同定、長期的な予後予測、さらには個別化医療の鍵となる治療薬の効果予測モデルの作成を行い、真に患者様に貢献できる精密診療の実装を目指します。
ヒトデータと疾患モデルの統合解析による「臓器相関」の解明
SLD(脂肪性肝疾患)は、腸・脳・筋肉・脂肪組織など多種多様な臓器と密接に関わり合う「全身性疾患」です。肝病態が心血管疾患や他臓器癌のリスクを増大させる一方で、他臓器の状態もまた肝病態の進展を左右します。 私たちは、ヒト臨床データから得られた知見を独自の疾患モデルマウスへとシームレスに繋げ、臓器間で交わされる未知の分子シグナルや細胞間ネットワークを解明します。肝臓局所にとどまらず、全身を一つの有機的なシステムとして捉えることで、従来の視点では到達できなかった病態の「新機軸」を同定し、全身状態の改善を見据えた次世代の治療戦略を切り拓きます。
創薬標的の同定から臨床応用へ向けた橋渡し研究
基礎研究で見出されたSLDの改善に資する分子標的や治療候補に対し、マウスモデルを用いた薬効・安全性評価を行います。特に、他臓器への波及効果も考慮した全身的な治療ベネフィットを検証し、基礎研究の成果を臨床研究へとスムーズに繋げるトランスレーショナルリサーチを展開します。最終的には、製薬企業や学術機関との連携を通じ、SLDおよびその関連合併症に悩む患者様へ新たな治療選択肢を提供することを目指します。
将来展望:Borderless Medicine: 多臓器ネットワーク解析が拓く次世代のSLD診療体系
本研究グループが目指すのは、SLDを単なる「肝臓の病」ではなく、「Systemic Disease(全身性疾患)」として捉え直し、新たな医療のあり方を提示することです。肝臓と他臓器の境界を取り払い、全身を一つの動的なネットワークとして解き明かすこと、さらには基礎研究と臨床現場の垣根をなくし、知見を双方向に循環させることを目指し、コンセプトとして「Borderless」を掲げています。私たちは、このネットワークの解明を通じて同定したバイオマーカーや治療標的を、滞ることなく社会実装へと繋げ、個々の病態に応じた精密な予測と介入を可能にする「次世代のSLD診療体系」を具体化していきたいと思っています。
【主要論文】
- Sakane S, Nishio T, Fuji H, Park SY, Ishizuka K, Miciano C, Kimura Y, Hosseini M, Diggle K, Zhang V, Lee W, Kim HY, Liu X, Wang A, Brenner DA, Kisseleva T. Msln/Muc16 signaling in activated Portal Fibroblasts drives the development of cholestatic fibrosis and HCC in aged female Mdr2-/- mice. Cell Mol Gastroenterol Hepatol. 2026 Apr 10:101785. doi: 10.1016/j.jcmgh.2026.101785
- Kogiso T, Akuta N, Ikejima K, Otsuka M, Kawaguchi T, Kawanaka M, Takahashi H, Tamaki N, Nakagawa H, Hikita H, Fujii H, Yamaguchi K, Yoneda M, Kon K, Uchiyama A, Seko Y, Sakane S, Shigefuku R, Fujiwara N, Iwaki M, Kobayashi T, Adachi T, Takeuchi Y, Tsutsumi T, Nakano, Shibayama K, Urata N, Miyaaki H, Kuroda H, Koseki M, Sone H, Matsubayashi Y, Kakisaka K, Takai A, Notsumata K, Seike M, Takei Y, Takeyama Y, Eguchi S, Watanabe S, Isomoto H, Yotsuyanagi H, Itoi T, Takehara T, Mochida S. Evidence-based clinical practice guidelines for metabolic dysfunction–associated steatotic liver disease (MASLD) 2026. Hepatol Res. in press
- Li D, Loneker AE, Safraou Y, Ford J, Mihelc E, Sakane S, Kisseleva T, Levental KR, Levental I, Sack I, Janmey PA, Wells RG. Cholesterol-containing lipid crystals can directly stiffen the rat steatotic liver before fibrosis. Proc Natl Acad Sci U S A. 2026 Jan 13;123(2):e2518060123.
- Ganguly S, Sakane S, Hokutan K, Zhang V, Miciano C, Wang A, Brenner DA, Kisseleva T. Aging and Aging-Related Senescence in Liver. Semin Liver Dis. 2025 Dec;45(4):549-566.
- Yamamoto G, Carvalho-Gontijo Weber R, Lee W, Zhang V, Jang H, Sakane S, Liu X, Kim HY, Brenner DA, Li N, Kisseleva T. DHCR7 inhibition ameliorates MetALD and HCC in mice and human 3D liver spheroids. JHEP Rep. 2025 Apr 5;7(7):101415.
- Sakane S, Hikita H. Revisiting the relationship between thyroid function and metabolic dysfunction-associated steatotic liver disease in the era of resmetirom. J Gastroenterol. 2025 Mar;60(3):389-391.
- Gu L, Zhu Y, Nandi SP, Lee M, Watari K, Bareng B, Ohira M, Liu Y, Sakane S, Carlessi R, Sauceda C, Dhar D, Ganguly S, Hosseini M, Teneche MG, Adams PD, Gonzalez DJ, Kisseleva T; Liver Cancer Collaborative; Tirnitz-Parker JEE, Simon MC, Alexandrov LB, Karin M. FBP1 controls liver cancer evolution from senescent MASH hepatocytes. Nature. 2025 Jan;637(8045):461-469.
- Sakane S, Hikita H, Shirai K, Sakamoto T, Narumi R, Adachi J, Kakita N, Yamada Y, Toyoda H, Takahashi H, Suda G, Kai M, Tahata Y, Sakamori R, Kumazaki S, Fukumoto K, Myojin Y, Murai K, Kodama T, Tatsumi T, Tomonaga T, Sakamoto N, Morii E, Takehara T. Proteomic analysis of serum extracellular vesicles reveals Fibulin-3 as a new marker predicting liver-related events in MASLD. Hepatol Commun. 2024 Jun 3;8(6):e0448.
- Osna NA, Tikhanovich I, Ortega-Ribera M, Mueller S, Zheng C, Mueller J, Li S, Sakane S, Weber RCG, Kim HY, Lee W, Ganguly S, Kimura Y, Liu X, Dhar D, Diggle K, Brenner DA, Kisseleva T, Attal N, McKillop IH, Chokshi S, Mahato R, Rasineni K, Szabo G, Kharbanda KK. Alcohol-Associated Liver Disease Outcomes: Critical Mechanisms of Liver Injury Progression. Biomolecules. 2024 Mar 27;14(4):404.
- Isaac R, Bandyopadhyay G, Rohm TV, Kang S, Wang J, Pokhrel N, Sakane S, Zapata R, Libster AM, Vinik Y, Berhan A, Kisseleva T, Borok Z, Zick Y, Telese F, Webster NJG, Olefsky JM. TM7SF3 controls TEAD1 splicing to prevent MASH-induced liver fibrosis. Cell Metab. 2024 May 7;36(5):1030-1043.e7.
- Kim HY, Sakane S, Eguileor A, Carvalho Gontijo Weber R, Lee W, Liu X, Lam K, Ishizuka K, Rosenthal SB, Diggle K, Brenner DA, Kisseleva T. The Origin and Fate of Liver Myofibroblasts. Cell Mol Gastroenterol Hepatol. 2024;17(1):93-106.
- Liu X, Lam K, Zhao H, Sakane S, Kim HY, Eguileor A, Diggle K, Wu S, Gontijo Weber RC, Soroosh P, Hosseini M, Mekeel K, Brenner DA, Kisseleva T. Isolation of primary human liver cells from normal and nonalcoholic steatohepatitis livers. STAR Protoc. 2023 Sep 15;4(3):102391.
- Sakane S, Hikita H, Shirai K, Myojin Y, Sasaki Y, Kudo S, Fukumoto K, Mizutani N, Tahata Y, Makino Y, Yamada R, Kodama T, Sakamori R, Tatsumi T, Takehara T. White Adipose Tissue Autophagy and Adipose-Liver Crosstalk Exacerbate Nonalcoholic Fatty Liver Disease in Mice. Cell Mol Gastroenterol Hepatol. 2021;12(5):1683-1699.
