消化管癌・内視鏡グループ
グループリーダー:辻井芳樹
コンセプト:内視鏡と科学を融合し、消化管癌診療の未来を創る
内視鏡診療を基盤とした高い臨床力と科学的思考力を融合し、消化管癌の診断・治療の進歩に貢献すべく、臨床に直結するエビデンスの創出に励んでいます。基礎から臨床まで幅広い研究を展開し、消化管癌の発生や進展機序の解明、新たな治療標的や有用なバイオマーカーの探索、高精度な診断技術や低侵襲治療法の開発に取り組んでいます。さらに、OGF(Osaka Gut Forum)をはじめとする研究組織を基盤に、多施設共同研究を積極的に推進し、得られた成果を臨床現場へ還元することで、より質の高い医療の実現を目指しています。
内視鏡を軸にした消化管癌診療の質的向上の追求
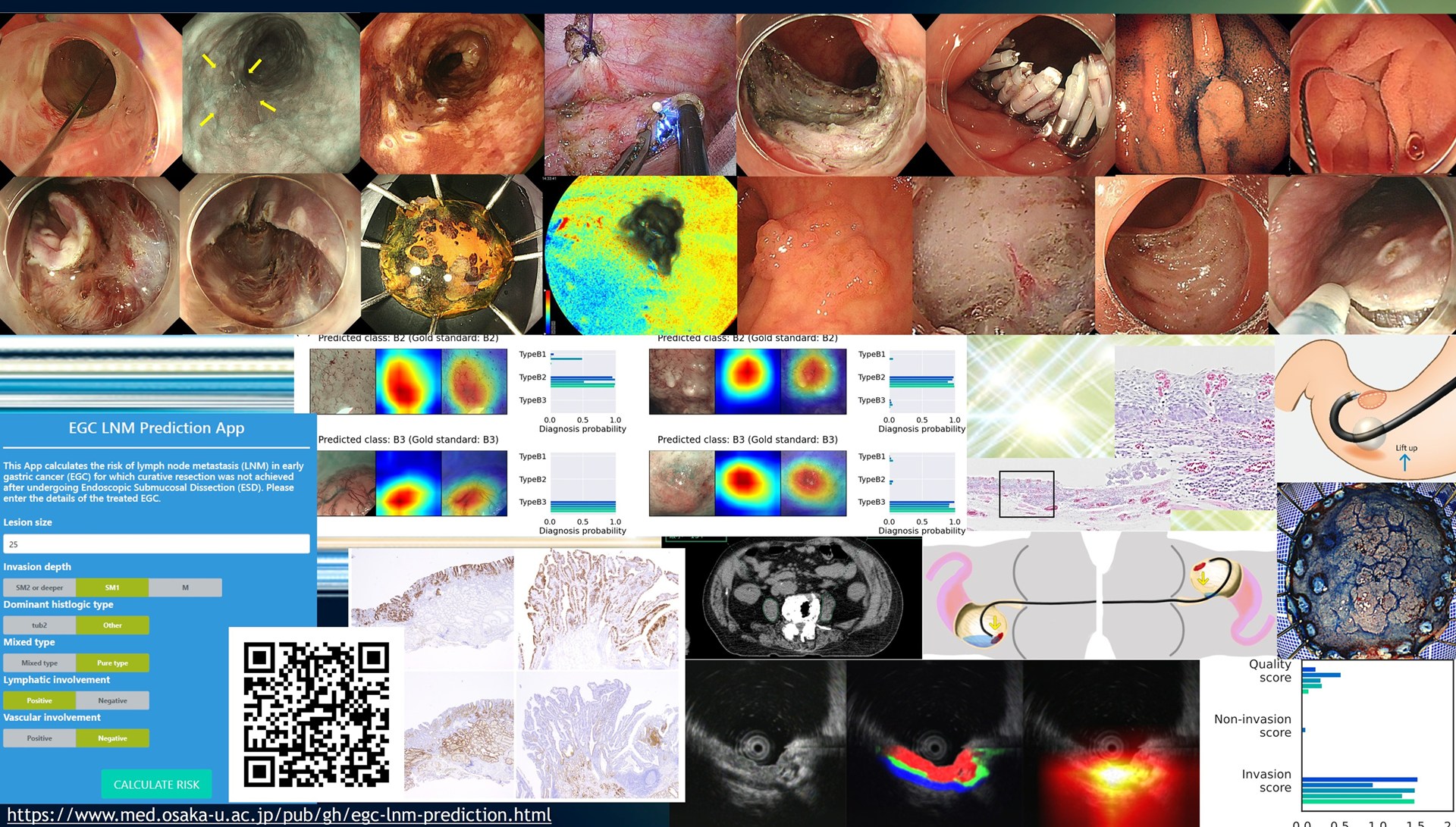
ESDを中心とした早期消化管癌に対する内視鏡治療の成績向上には、正確な診断と適切な治療手段の選択が不可欠です。そのため、私たちは、高精度な診断技術の開発と、高精度な診断に基づく最適な治療戦略の確立を目指しています。さらに、安全かつ確実な根治を実現するため、手技の精緻化に努めるとともに、より低侵襲な新規内視鏡治療の開発にも取り組んでいます。内視鏡治療のみならず、バイオマーカー測定や遺伝子パネル検査を踏まえた多彩な薬物療法、放射線治療等による集学的治療を行う過程で得られた臨床検体とデータを最大限に活用し、AIも駆使しながら、がん診療の質的向上を追求しています。 これまでにも、消化管癌の診断に関する検討1-3)、消化管癌に対する低侵襲治療法の評価4-5)と新規治療の開発6-7)、集学的治療に関する検討8-9)等について報告しています。
多施設共同研究によるリアルワールドエビデンスの創出
臨床の現場から生まれるクリニカルクエスチョンを出発点に、現在の臨床的課題を解決するための多施設共同研究を積極的に推進しています。私たちのグループは、阪大関連施設との強固なネットワークを構築し、OGF(Osaka Gut Forum)を研究基盤として多角的な研究を主導し、エビデンスの創出と発信を行っています。 これまでに、AIを用いたEUS深達度診断モデル10)やリンパ節転移予測モデル11)の構築、ESD後出血予防策の提唱12)、ESD後長期成績についての検証13-14)、十二指腸腺腫の発育進展についての検討15)などを報告しています。
内視鏡診療に根ざした基礎・橋渡し研究の深化
臨床病理学的検討や分子生物学的解析により、消化管癌の発生・進展機序の解明や新規治療標的、有用なバイオマーカーの探索につながる基礎・橋渡し研究を展開しています。 これまでに、胃癌範囲診断を困難にする要因16)、大腸癌進展を促進する癌細胞―間質相互作用の機序17-20)を明らかにし報告しています。
将来展望:消化管癌を制御する時代へー診断・治療・予測の統合的進化ー
内視鏡を中核とした診断と治療を今後さらに科学的に発展させ、消化管癌診療の質の向上と最適化を目指します。AI診断、バイオマーカーを統合した多層的診断体系の確立と、新規の治療標的やバイオマーカーの開発を進めます。多施設共同研究ネットワークをさらに強化し、観察研究で得られた知見を前向き介入研究へと発展させることで、診療を変えるエビデンスを創出し、消化管癌を「制御できる疾患」へと変革していきます。
【主要論文】
- Tsujii Y, Hayashi Y, Ishihara R, Yamaguchi S, Yamamoto M, Inoue T, Nagai K, Ogiyama H, Yamada T, Nakahara M, Kizu T, Kanesaka T, Matsuura N, Ohta T, Nakamatsu D, Yoshii S, Shinzaki S, Nishida T, Iijima H, Takehara T. Diagnostic value of endoscopic ultrasonography for the depth of gastric cancer suspected of submucosal invasion: a multicenter prospective study. Surg Endosc. 2023 Apr;37(4):3018-3028.
- Uema R, Hayashi Y, Tashiro T, Saiki H, Kato M, Amano T, Tani M, Yoshihara T, Inoue T, Kimura K, Iwatani S, Sakatani A, Yoshii S, Tsujii Y, Shinzaki S, Iijima H, Takehara T. Use of a convolutional neural network for classifying microvessels of superficial esophageal squamous cell carcinomas. J Gastroenterol Hepatol. 2021 Aug;36(8):2239-2246.
- Tsujii Y, Kato M, Inoue T, Yoshii S, Nagai K, Fujinaga T, Maekawa A, Hayashi Y, Akasaka T, Shinzaki S, Watabe K, Nishida T, Iijima H, Tsujii M, Takehara T. Integrated diagnostic strategy for the invasion depth of early gastric cancer by conventional endoscopy and EUS. Gastrointest Endosc. 2015 Sep;82(3):452-9.
- Adachi Y, Hayashi Y, Yoneda S, Tajiri A, Fukuda H, Kimura E, Nakagawa K, Saiki H, Uema R, Yoshihara T, Tsujii Y, Takehara T. Outcomes of additional chemotherapy for esophageal squamous cell carcinoma following non-curative endoscopic submucosal dissection. Int J Clin Oncol. 2025 Dec;30(12):2567-2575.
- Tsujii Y, Hayashi Y, Uema R, Saiki H, Kimura E, Nakagawa K, Fukuda H, Tajiri A, Adachi Y, Yoshihara T, Inoue T, Kato M, Yoshii S, Suzuki M, Makino T, Takehara T. Feasibility and safety of endoscopic submucosal dissection for superficial cancer of the remnant esophagus after esophagectomy. Esophagus. 2025 Apr;22(2):148-156.
- Tsujii Y, Yamasaki M, Hayashi Y, Tanaka K, Makino T, Doki Y, Takehara T. Thoracoscopic and endoscopic cooperative surgery (TECS): a novel less invasive technique for resection of gastric tube cancer after esophagectomy. Endoscopy. 2019 Jan;51(1):E5-E6.
- Yoshii S, Akasaka T, Hayashi Y, Tsujii Y, Nagai K, Higashino K, Ishihara R, Iijima H, Takehara T. “Underwater” endoscopic submucosal dissection: a novel method for resection in saline with a bipolar needle knife for colorectal epithelial neoplasia. Surg Endosc. 2018 Dec;32(12):5031-5036.
- Nakagawa K, Hayashi Y, Adachi Y, Tajiri A, Fukuda H, Kimura E, Uema R, Saiki H, Kato M, Inoue T, Yoshihara T, Yoshii S, Tsujii Y, Takehara T. Low skeletal muscle mass contributes to the prognosis of patients with superficial esophageal cancer treated with definitive chemoradiotherapy. Esophagus. 2025 Apr;22(2):198-206.
- Hayashi Y, Iijima H, Isohashi F, Tsujii Y, Fujinaga T, Nagai K, Yoshii S, Sakatani A, Hiyama S, Shinzaki S, Makino T, Yamasaki M, Ogawa K, Doki Y, Takehara T. The heart’s exposure to radiation increases the risk of cardiac toxicity after chemoradiotherapy for superficial esophageal cancer: a retrospective cohort study. BMC Cancer. 2019 Mar 4;19(1):195.
- Uema R, Hayashi Y, Kizu T, Igura T, Ogiyama H, Yamada T, Takeda R, Nagai K, Inoue T, Yamamoto M, Yamaguchi S, Kanesaka T, Yoshihara T, Kato M, Yoshii S, Tsujii Y, Shinzaki S, Takehara T. A novel artificial intelligence-based endoscopic ultrasonography diagnostic system for diagnosing the invasion depth of early gastric cancer. J Gastroenterol. 2024 Jul;59(7):543-555.
- Kato M, Hayashi Y, Uema R, Kanesaka T, Yamaguchi S, Maekawa A, Yamada T, Yamamoto M, Kitamura S, Inoue T, Yamamoto S, Kizu T, Takeda R, Ogiyama H, Yamamoto K, Aoi K, Nagaike K, Sasai Y, Egawa S, Akamatsu H, Ogawa H, Komori M, Akihiro N, Yoshihara T, Tsujii Y, Takehara T. A machine learning model for predicting the lymph node metastasis of early gastric cancer not meeting the endoscopic curability criteria. Gastric Cancer. 2024 Sep;27(5):1069-1077.
- Ogiyama H, Kato M, Yamaguchi S, Kanesaka T, Yamada T, Yamamoto M, Komori M, Nagaike K, Nakahara M, Tsutsui S, Tsujii Y, Saita R, Iijima H, Hayashi Y, Takehara T. Efficacy of prophylactic clip closure in reducing the risk of delayed bleeding after colorectal endoscopic submucosal dissection in patients on anticoagulant therapy: Multicenter prospective study. Dig Endosc. 2024 Sep;36(9):1021-1029.
- Tajiri A, Tsujii Y, Nishida T, Inoue T, Maekawa A, Kitamura S, Yamaguchi S, Nishihara A, Yamada T, Ogiyama H, Murayama Y, Yamamoto S, Egawa S, Uema R, Yoshihara T, Hayashi Y, Takehara T. High incidence of lung cancer death after curative endoscopic submucosal dissection for superficial esophageal squamous cell carcinoma. Cancer Med. 2024 May;13(9):e7242.
- Kato M, Hayashi Y, Fukuda H, Yamaguchi S, Inoue T, Ogiyama H, Kitamura S, Komori M, Yamamoto K, Yamamoto M, Nagai K, Nakahara M, Egawa S, Yamada T, Sasakawa A, Kizu T, Nishiyama O, Shichijo S, Yoshii S, Tsujii Y, Shinzaki S, Iijima H, Takehara T. Geriatric nutritional risk index as a prognostic indicator in elderly patients with early colorectal cancer undergoing endoscopic submucosal dissection. Dig Endosc. 2022 Mar;34(3):569-578.
- Uema R, Hayashi Y, Komori M, Shibukawa N, Hayashi N, Horimoto M, Yamada T, Yamamoto M, Hiyama S, Kinoshita K, Ogiyama H, Yamaguchi S, Egawa S, Kanesaka T, Kato M, Yoshii S, Tsujii Y, Keiichiro H, Shinzaki S, Iijima H, Morii E, Takehara T. Non-Pure Intestinal Phenotype as an Indicator of Progression in Sporadic Nonampullary Duodenal Adenomas: A Multicenter Retrospective Cohort Study. Clin Transl Gastroenterol. 2024 Jan 1;15(1):e00649.
- Nagai K, Hayashi Y, Uema R, Inoue T, Kimura K, Sakatani A, Yoshii S, Tsujii Y, Shinzaki S, Iijima H, Takehara T. Clinical and Histopathological Features of the Differentiated Type of Early Gastric Cancer with an Unclear Lateral Demarcation. Digestion. 2022;103(5):347-356.
- Kimura E, Hayashi Y, Nakagawa K, Saiki H, Kato M, Uema R, Inoue T, Yoshihara T, Sakatani A, Fukuda H, Tajiri A, Adachi Y, Murai K, Yoshii S, Tsujii Y, Shinzaki S, Iijima H, Takehara T. p53 Deficiency in Colon Cancer Cells Promotes Tumor Progression Through the Modulation of Meflin in Fibroblasts. Cancer Sci. 2025 Jul;116(7):1871-1882.
- Saiki H, Hayashi Y, Yoshii S, Kimura E, Nakagawa K, Kato M, Uema R, Inoue T, Sakatani A, Yoshihara T, Tsujii Y, Shinzaki S, Iijima H, Takehara T. The apelin apelin receptor signaling pathway in fibroblasts is involved in tumor growth via p53 expression of cancer cells. Int J Oncol. 2023 Dec;63(6):139.
- Inoue T, Hayashi Y, Tsujii Y, Yoshii S, Sakatani A, Kimura K, Uema R, Kato M, Saiki H, Shinzaki S, Iijima H, Takehara T. Suppression of autophagy promotes fibroblast activation in p53-deficient colorectal cancer cells. Sci Rep. 2021 Sep 30;11(1):19524.
- Yoshii S, Hayashi Y, Iijima H, Inoue T, Kimura K, Sakatani A, Nagai K, Fujinaga T, Hiyama S, Kodama T, Shinzaki S, Tsujii Y, Watabe K, Takehara T. Exosomal microRNAs derived from colon cancer cells promote tumor progression by suppressing fibroblast TP53 expression. Cancer Sci. 2019 Aug;110(8):2396-2407.
