Non-mitogenic CD3抗体によるT細胞受容体発現量低下を介したマウスループス軽減効果
Front Immunol 2022; 13: 855812. PMID: 35419004
Reduction of Cell Surface T-cell Receptor by Non-mitogenic CD3 Antibody to Mitigate Murine Lupus
Morita M, Mizui M, Masuyama S, Tsokos GC, Isaka Y.
Tリンパ球は全身性エリテマトーデス(SLE)の病態・進展において重要な役割を果たします。抗CD3抗体は、過去に移植後免疫抑制剤として使用され、SLEを含む様々な自己免疫疾患で有効性が示唆されているものの、生体内での抗体活性が多面的であり、詳細な免疫抑制機構が不明瞭な点が多いままです。本研究では従来の抗CD3抗体(conventional 2C11, 2C11C)とFc受容体および補体結合能を欠失した組み換え抗CD3抗体(silent 2C11, 2C11S)を比較検討し、その作用機序を明らかにしました。2C11Sの2C11Cと比較した相違点については、①T細胞受容体(TCR)発現量低下を長期間持続させ、②一時的なインテグリンの活性化により末梢血管などにリンパ球をトラップさせるが、③サイトカインリリース症候群やT細胞消失を誘導しないことから、2C11Sのin vivoにおける有効性・安全性が示されました。次にマウスSLE自然発症モデルであるNZB/W F1マウスにCD3抗体を初期(10週齢)、後期(20週齢)に分けて週1回1ヶ月間投与し治療効果を検討したところ、ループス初期の2C11S治療は、胚中心B細胞減少および自己抗体産生を抑制し、後期の2C11S治療は、自己抗体や制御性T細胞・エフェクターT細胞分化に影響を与えることなく腎炎を抑制しました(図1)。
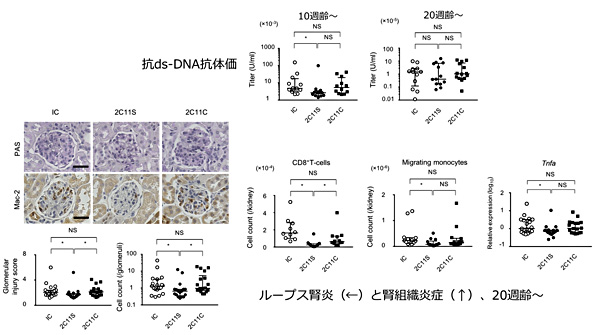
図1.CD3抗体によるマウスSLE/ループス腎炎治療効果
一方、2C11Cでは、短期治療による有効性は確認できませんでした。また、長期間投与によって2C11Sは重症ネフローゼ発症や死亡率を低減させることがわかりました(図2)。さらに、ループス進展に対するTCR発現量低下の影響を調べるため、T細胞表面TCR発現量のみ低下し、正常なT細胞発生・TCRシグナル応答を示すCd3z+/- マウスを用いたところ、ループスモデルのB6lprマウスにおいてB6lpr-Cd3z+/- マウスの自己抗体産生およびループス腎炎進行がB6lpr-CD3z+/+ マウスに比して有意に抑制されることを確認しました。以上より、non-mitogenic抗CD3抗体投与によって、ループスの病態は抑制され、その作用は主としてT細胞表面TCR発現量低下を介した免疫抑制効果であることが示唆されました。サイレント型CD3抗体はヒト自己免疫疾患に対して有効性が見直されつつあり、本研究は臨床応用に向けてその機序的な面からも貢献できるかもしれません。
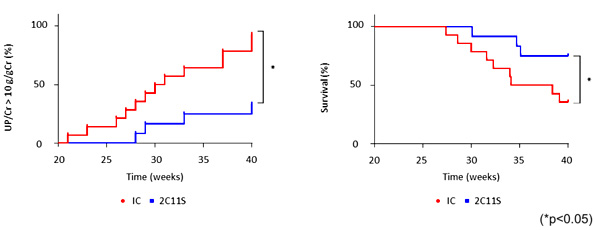
図2.2C11S投与によるループス腎炎(重症ネフローゼ)抑制および生存率改善
