|
芽細胞発癌 Fetal Cell Carcinogenesis
|
Go to English Page
1. がんの発生母地は何か?を考えた時点で多段階発癌説は崩壊する
40年以上にわたり、癌は正常細胞が遺伝子(DNA)の変異を起こし、癌抑制遺伝子や癌遺伝子の活性に変化をきたすことで増殖能が増し、生体内でセレクションを受けることで転移能や浸潤能といった悪性形質を獲得(プログレッション)して発生するという多段階発癌説(multi-step carcinogenesis)が信じられてきました。例えば下の図のような考え方です。
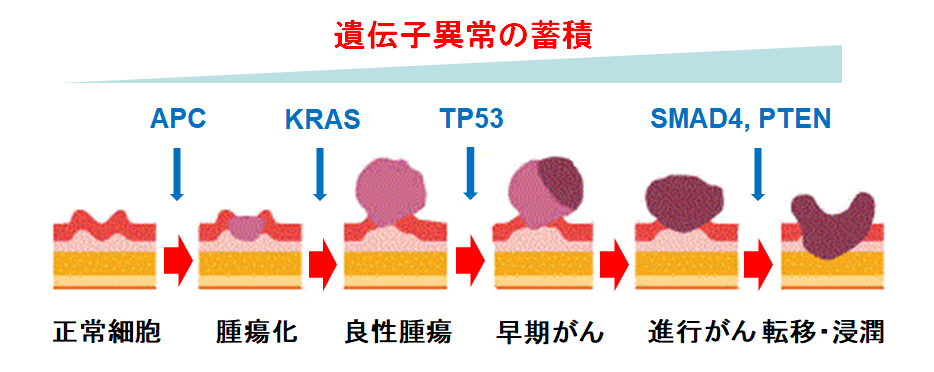 しかしこの考え方は根本的な問題を抱えています。”正常細胞”って何なんでしょうか。たとえば、甲状腺なら、成人で見られる甲状腺濾胞上皮細胞を指しているのでしょうか。多段階発癌を説明している教科書で、この疑問に真っ向から答えているものは実はあまり多くありません。このことを持ち出すと説明がやりにくくなるからです。すべての細胞は臓器発生初期に存在する幹細胞等の胎児性細胞から分化して産生されます。これらの胎児性細胞から癌が発生する可能性は無いのでしょうか。「ない」、と否定してしまうのははなはだ困難でしょう。しかし、可能性があるのだ、としてしまうと、次のことを考えないとなりません。、すなわち、発癌のスタートである発生母地の細胞の性質が異なるなら、その後の発癌過程も異なるであろうということです。特に、発生初期の「正常な細胞」である幹細胞等は活発に増殖しかつ癌の転移能に相当する移動能を持っています。すなわち癌細胞にそっくりな細胞です。これらの細胞から癌が発生するのであれば、従来言われていた悪性化の過程(プログレッション)は必要ありません。これらの胎児性細胞がその性質を維持したまま増殖できたらよいのでワンステップで非常に簡単に癌が発生することになります。従来の多段階発癌説ではこのようなシンプルな経路をなぜか無視して、胎児性細胞がいったん分化して癌形質を失い、先祖返りで脱分化してに癌形質を再び獲得する、という複雑な過程を経ている、としてきたのです。臓器発生初期の胎児性細胞から直接癌が発生する、これが我々が2000年の国際甲状腺学会で世界で初めて報告した芽細胞発癌説(fetal
cell carcinogenesis)の基本概念です。”正常細胞”って何だろう?という疑問に気づいてしまうと、多段階発癌説は成立させるのがもはや困難になってしまいます。多段階発癌説の創成期に活躍したBert Vogelsteinは最近、Scienceで「癌は幹細胞以外からは発生しない*」という論文を書いています(Science
355:1330-34, 2015)。おそらくこのような理論的矛盾に気づいたのだと思います。
しかしこの考え方は根本的な問題を抱えています。”正常細胞”って何なんでしょうか。たとえば、甲状腺なら、成人で見られる甲状腺濾胞上皮細胞を指しているのでしょうか。多段階発癌を説明している教科書で、この疑問に真っ向から答えているものは実はあまり多くありません。このことを持ち出すと説明がやりにくくなるからです。すべての細胞は臓器発生初期に存在する幹細胞等の胎児性細胞から分化して産生されます。これらの胎児性細胞から癌が発生する可能性は無いのでしょうか。「ない」、と否定してしまうのははなはだ困難でしょう。しかし、可能性があるのだ、としてしまうと、次のことを考えないとなりません。、すなわち、発癌のスタートである発生母地の細胞の性質が異なるなら、その後の発癌過程も異なるであろうということです。特に、発生初期の「正常な細胞」である幹細胞等は活発に増殖しかつ癌の転移能に相当する移動能を持っています。すなわち癌細胞にそっくりな細胞です。これらの細胞から癌が発生するのであれば、従来言われていた悪性化の過程(プログレッション)は必要ありません。これらの胎児性細胞がその性質を維持したまま増殖できたらよいのでワンステップで非常に簡単に癌が発生することになります。従来の多段階発癌説ではこのようなシンプルな経路をなぜか無視して、胎児性細胞がいったん分化して癌形質を失い、先祖返りで脱分化してに癌形質を再び獲得する、という複雑な過程を経ている、としてきたのです。臓器発生初期の胎児性細胞から直接癌が発生する、これが我々が2000年の国際甲状腺学会で世界で初めて報告した芽細胞発癌説(fetal
cell carcinogenesis)の基本概念です。”正常細胞”って何だろう?という疑問に気づいてしまうと、多段階発癌説は成立させるのがもはや困難になってしまいます。多段階発癌説の創成期に活躍したBert Vogelsteinは最近、Scienceで「癌は幹細胞以外からは発生しない*」という論文を書いています(Science
355:1330-34, 2015)。おそらくこのような理論的矛盾に気づいたのだと思います。
*甲状腺癌に関していえば、幹細胞以外からも癌が発生すると考えられます。それが後で述べるSelf-limiting
Cancerです。
2.芽細胞発癌説で見る甲状腺癌の発生メカニズム
 発生初期の甲状腺では3種類の胎児性細胞が確認できます。甲状腺は胎生期に舌根部で小さな細胞の塊として最初に現れます。これが甲状腺幹細胞(thyroid
stem cell)です。この細胞は前頸部に向けて移動を開始し、成長しつつ甲状腺特異的蛋白であるサイログロブリンを発現する細胞に変化します。これが甲状腺芽細胞(thyroblast)です。甲状腺幹細胞と芽細胞は癌形質の1つである移動能(転移能・浸潤能に相当)を有していることがわかります。さらに前頸部に落ち着く頃には甲状腺組織の特徴である濾胞を形成する細胞に変化します。これが前甲状腺細胞(prothyrocyte)です。芽細胞発癌説ではこれら3種類の胎児性細胞が遺伝子変異等何らかの原因で分化を止めた時に甲状腺腫瘍が発生します。芽細胞発癌説では”発癌”という現象は広い意味での発生異常として捉えることができます。
発生初期の甲状腺では3種類の胎児性細胞が確認できます。甲状腺は胎生期に舌根部で小さな細胞の塊として最初に現れます。これが甲状腺幹細胞(thyroid
stem cell)です。この細胞は前頸部に向けて移動を開始し、成長しつつ甲状腺特異的蛋白であるサイログロブリンを発現する細胞に変化します。これが甲状腺芽細胞(thyroblast)です。甲状腺幹細胞と芽細胞は癌形質の1つである移動能(転移能・浸潤能に相当)を有していることがわかります。さらに前頸部に落ち着く頃には甲状腺組織の特徴である濾胞を形成する細胞に変化します。これが前甲状腺細胞(prothyrocyte)です。芽細胞発癌説ではこれら3種類の胎児性細胞が遺伝子変異等何らかの原因で分化を止めた時に甲状腺腫瘍が発生します。芽細胞発癌説では”発癌”という現象は広い意味での発生異常として捉えることができます。
甲状腺幹細胞と芽細胞は移動能を有しているので、これらから発生した腫瘍は癌としてふるまうのに対し、移動能を失った前甲状腺細胞からは良性腫瘍のみが発生します。幹細胞は無限の増殖能を持っています。したがって、甲状腺幹細胞から発生した癌は無限に増殖して患者を殺します(Lethal
Cancer)。未分化癌や予後の悪い分化癌(乳頭癌・濾胞癌)がこれに相当します。これに対して甲状腺芽細胞と前甲状腺細胞は、増殖力には限りがありますから、いずれ成長を止めます。ここで興味深い現象があります。甲状腺芽細胞から発生した癌は、転移能・浸潤能を有する立派な癌です。ところが、成長に限りがあり、いずれ増殖を止めるので滅多に患者を殺すことはありません。これをSelf-limiting
Cancerと呼びます。成人で見られる微小乳頭癌や若年者の甲状腺癌がこれに相当します。
腫瘍の成長パターンについても興味深い考察ができます。幹細胞は長期間成長を止めた静止状態を維持することができますが、その他の細胞は静止することができないので発生したらすぐに分裂を開始します。したがって、甲状腺腺芽細胞と前甲状腺細胞由来の予後良い腫瘍は若年期に臨床的な腫瘍となりますが、甲状腺幹細胞から発生する予後の悪い癌は中年以降に臨床癌となります。癌の発生母地となる甲状腺幹細胞と芽細胞は5歳ころには消失すると考えられます。5歳以降は発癌誘導ができないからです。
3.芽細胞発癌説で見た甲状腺癌の自然史
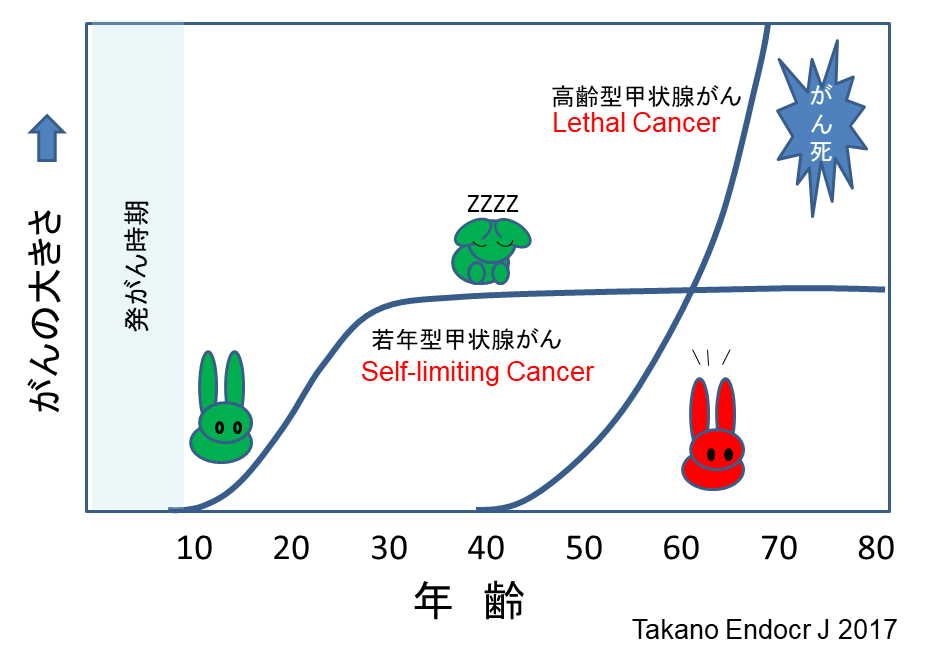 芽細胞発癌では甲状腺癌の最初の発生は甲状腺組織が発生してから発生母地である胎児性細胞がまだ残っている5歳までの間であるとしています。甲状腺芽細胞から発生する癌は成長に限りがあるSelf-limiting
Cancerです。これを若年型甲状腺癌と呼びます。若年型甲状腺癌は10-20代で急速に成長し、転移・浸潤もきたします。一部はこの時期に臨床癌となり、首の結節等で見つかりますが、成長に限りがあるため滅多に患者を殺すことはありません。大部分の癌はそこまで成長せず、超音波検査でしか見つけることができない潜在癌として一生経過します。若年型甲状腺癌を早く見つけてもそのほとんどが生涯悪さをすることが無いので患者にメリットはありません。患者に悪さをすることがはっきりした時点で治療を考える、といった性質の癌です。
芽細胞発癌では甲状腺癌の最初の発生は甲状腺組織が発生してから発生母地である胎児性細胞がまだ残っている5歳までの間であるとしています。甲状腺芽細胞から発生する癌は成長に限りがあるSelf-limiting
Cancerです。これを若年型甲状腺癌と呼びます。若年型甲状腺癌は10-20代で急速に成長し、転移・浸潤もきたします。一部はこの時期に臨床癌となり、首の結節等で見つかりますが、成長に限りがあるため滅多に患者を殺すことはありません。大部分の癌はそこまで成長せず、超音波検査でしか見つけることができない潜在癌として一生経過します。若年型甲状腺癌を早く見つけてもそのほとんどが生涯悪さをすることが無いので患者にメリットはありません。患者に悪さをすることがはっきりした時点で治療を考える、といった性質の癌です。
甲状腺幹細胞から発生する癌は無限の増殖能を持つLethal
Cancerです。これを高齢型甲状腺癌と呼びます。この癌は従来の癌のイメージに合致する腫瘍です。5歳までには発生していますが、臨床癌として現れるのは中年以降です。なぜそうなるのかは良くわかっていませんが、5歳以上で放射線を浴びても甲状腺癌の頻度は増えませんので従来言われてきたような遺伝子異常の外因的な蓄積が臨床癌に変化する原因ではないことは確実です。幹細胞の特性としてある程度年数が経たないと本格的な増殖過程に入れないのではないかと考えられています。すなわち、幹細胞の老化が癌の発生メカニズムの重要な要因であることが考えられます。この癌は早期に発見して治療しないと患者を殺してしまいますので早期診断・早期治療は有効です。
甲状腺癌は成長が遅いので”カメ”であると言われてきました。しかし、実はカメではありません。若年型甲状腺癌は最初はウサギのように活発に活動しますが、中年以降は成長を止めます。すなわち”昼寝するウサギ”です。これに対して、高齢型甲状腺癌はずっと成長を続ける”ウサギ”です。中高年では通常のウサギが休眠状態になってしまった多数の”昼寝ウサギ”に混じってしまうので、平均するといかにもカメのように見えてしまうのです。
4.芽細胞発癌説は甲状腺癌の謎を解決する
Q 甲状腺癌はなせ予後が良いのか?
甲状腺癌は実際は通常の「癌}である高齢型甲状腺癌と、患者を滅多に殺さない若年型甲状腺癌のミックスです。高齢型甲状腺癌の予後はそれほど良くないのですが、場合によっては治療さえ不要な若年型甲状腺癌が多数を占めるため、一見予後が良いように見えます。
Q なぜ高齢者になるほど甲状腺癌の予後は悪いのか?
高齢型甲状腺癌の占める割合が増えるからです。40歳未満ではほぼ全例が若年型と考えられます。
Q 甲状腺癌はなぜ女性に多いのか?
甲状腺癌の発生母地は胎生期に存在する胎児性細胞です。これらの細胞は母胎内で女性ホルモンが高い環境下で活発に増殖する細胞です。従って、男性よりも女性で成長しやすいことが予測できます。
Q 甲状腺癌で転移している患者でも予後が良いのはなぜか?
胎児性甲状腺細胞は、高い移動能を持ちますが、甲状腺のサイズを考えればわかる通り、増殖力はそれほど強くありません。したがってこのような細胞から発生した腫瘍は、派手に転移はするものの成長の遅い癌となります。
5.多段階発癌が正しいのか、芽細胞発癌が正しいのか、エビデンスを見てみよう
「芽細胞発癌はまだ証明されてない」 これは今でも良く語られる言葉です。癌の発生メカニズムを証明することは容易ではありません。特に、芽細胞発癌説では癌死をもたらすような癌は胎生期に存在する幹細胞が何十年もかかって老化して発生する、としていますから、それを直接的に証明するのははなはだ困難です。このような事情が多段階発癌説をながらえさせてきた、とも言えるでしょう。しかし翻って、何をもって多段階発癌が証明されていると信じてきたのでしょうか。実際は多段階発癌が「証明された」ことは甲状腺に関しては今まで一度もなかったといって良いでしょう。笑い話で「多段階発癌説の最強のエビデンスは偉い先生がそう言っていることだ」とも言われています。良く出てくるのは甲状腺未分化癌が分化癌から発生する、という事実ですが、これを多段階発癌説の根拠とするのは大きな間違いであることは後で述べます。多段階発癌説を唱える研究者たちも最近は解釈にさまざまな変更を加えており、多少ややこしくなっています。以下では、多段階発癌説の定義を教科書に書かれているとおり、「甲状腺癌は中年以降正常な濾胞上皮細胞が遺伝子異常の蓄積を起こして段階的に悪性化して発生する」としたものだとしておきましょう
(adenoma-carcinoma sequenceとした方が良いかもしれません)。ここで書かれているエビデンスを示す論文等は下記の参考文献に載っています。
検証1 甲状腺癌は中年以降発生するのか?
福島県民健康調査で、未成年に小さな甲状腺癌が高頻度で見つかったことは関係者に衝撃を与えました。全くの予想外であったからです。逆に言うと多段階発癌説に基づき、子供には甲状腺癌は存在しないと信じていたからこそ、このプロジェクトが実施されることになったのでしょう。20歳の段階で1000人に1人程度の頻度で既に甲状腺癌は存在しています。剖検例での解析では小さな甲状腺癌は10歳を超えると急激に頻度が上昇し、30歳代でいったんピークを迎えます。従って、甲状腺癌発生の第1波は幼少期で間違いありません。剖検例では潜在癌の頻度は60歳以降で再びゆっくり上昇してきます。ですから、40歳代以降に第2波があるのかもしれません。このデータは2峰性の発癌を予想する芽細胞発癌説に合致し、「中年以降」発生するという考えは間違いであることが分かります。
検証2 甲状腺癌は濾胞上皮細胞から発生するのか?
臨床的な事実として、放射性ヨウ素や放射線の外照射によって甲状腺癌の頻度が上昇するのは幼少期のみです。また、実験的事実からは、がん遺伝子をマウスの甲状腺に導入して甲状腺癌の発生をみることができるの胎生期のみです。これらの結果について多段階発癌を信じる研究者たちは、成人でも放射線による発癌リスクは”わずかに”ある、”工夫をすれば”大人のマウスでも甲状腺癌を発生させることは可能である、と言っています。しかし、それらはあくまで「例外的」な事象であり、原則は甲状腺癌の発がん誘導は成人ではできない、で間違いありません。 このことは、甲状腺癌の発生母地が成人ではもはや存在しないことを示しており、すなわち甲状腺癌は濾胞上皮細胞からは発生しません。
検証3 甲状腺癌は遺伝子異常の蓄積で悪性化しているのか?
臨床的な事実として良性の甲状腺腫瘍、濾胞腺腫等が乳頭癌等の癌に変わる現象は確認されていません。韓国で甲状腺超音波検査が普及した結果、小さな甲状腺癌が多数手術されましたが、甲状腺癌の死亡率は低下しませんでした。これらの小さな癌が癌死を引き起こすような癌に”進化”することは滅多にないことが分かります。また、微小乳頭癌で経過観察をされた例では、いまだに死亡例や未分化癌に変化した症例は皆無です。小さな大人しい甲状腺癌が悪性化することは、あるとしても極めて稀であると言えます。
また、分化癌が未分化癌にプログレッションしていく、ということが言われてきましたが、これについての証明はされていません。遺伝子異常の蓄積で未分化癌が発生するなら、分化癌で起こった遺伝子異常は未分化癌に引き継がれなければなりません。未分化癌だけで高頻度に異常が検出される遺伝子(TP53など)の存在がその根拠とされてきました。ところが、RET-PTC,
BRAF,
PAX8-PPARγ1、RAS等、分化癌で高頻度の異常を認めるものの、未分化癌では異常が見つからない、あるいは異常の頻度が激減する遺伝子も多数あります。どうしてこういうことになっているのか、については多段階発癌を唱える研究者たちは説明を避けてきました。
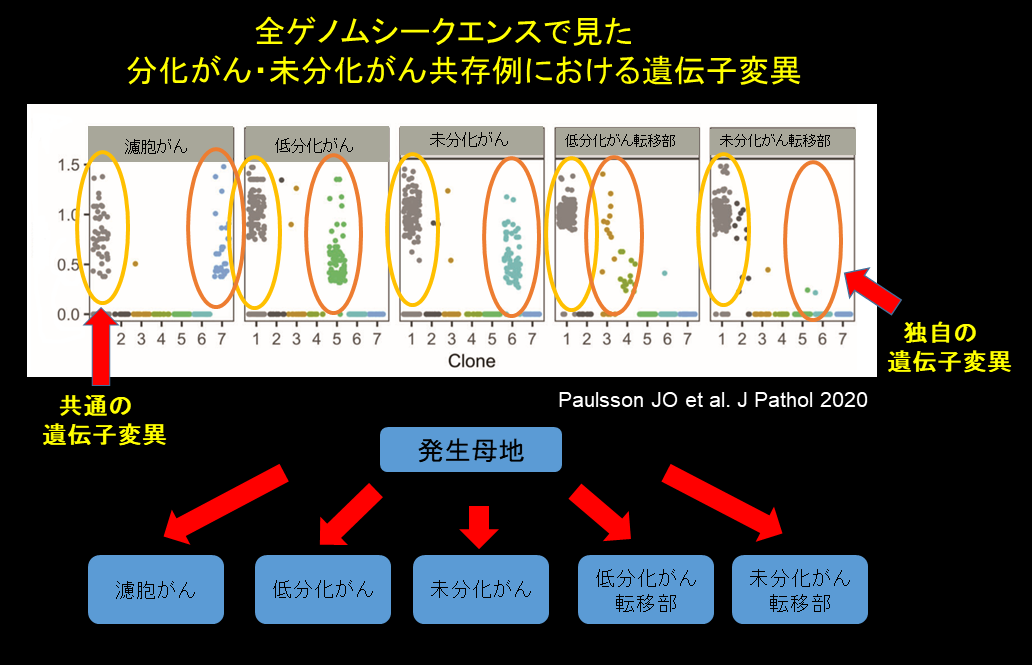 この謎については、最近、全ゲノム・エクソーム解析のデータが出てきて何が起こっているのかようやくはっきりわかってきました。現在までに3つの論文がでていますが、いずれも同じ結果です。この図は、分化癌である濾胞癌と低分化癌、未分化癌の同一症例における共存例について全ゲノム解析でそれぞれの腫瘍の遺伝子異常を検出したものです。従来このような症例は、最初に濾胞癌があって、そこから低分化癌が発生し、さらに低分化癌から未分化癌が発生した、と考えてきました。そうであれば、濾胞癌で存在する遺伝子異常は低分化癌に引き継がれ、低分化癌で存在する遺伝子異常はさらに未分化癌に引き継がれなければなりません。では、実際のデータはどうでしょうか。たしかに、すべての腫瘍に共通する遺伝子異常は存在しました。すなわち、これらの腫瘍は共通の発生母地を持つということです。ところが、濾胞癌・低分化癌・未分化癌のそれぞれが、多数の”独自の”遺伝子異常を有していたのです。すなわちこれらの腫瘍は共通の発生母地からまったく独自に進化をとげてきた、ということで1つの腫瘍から他の腫瘍へのプログレッションの形跡は認められません。これは多段階発癌を否定する動かぬ証拠です。また、濾胞癌が独自の遺伝子異常を多数有していることに注目してください。濾胞癌は年単位でゆっくりと成長するのに対して未分化癌は週単位で激しく増殖します。変異の発生頻度が増殖スピードと相関しているとすれば、濾胞癌は何年もかけてこれらの遺伝子異常を獲得したのに対して、未分化癌が変異を獲得したのはごく最近ということになります。芽細胞発癌で予想されたように、予後の良い癌が早期に増殖を開始するのに対し、悪性度の高い癌はサイレントのまま年単位で潜伏し、その後突然出てくることが分かります。
この謎については、最近、全ゲノム・エクソーム解析のデータが出てきて何が起こっているのかようやくはっきりわかってきました。現在までに3つの論文がでていますが、いずれも同じ結果です。この図は、分化癌である濾胞癌と低分化癌、未分化癌の同一症例における共存例について全ゲノム解析でそれぞれの腫瘍の遺伝子異常を検出したものです。従来このような症例は、最初に濾胞癌があって、そこから低分化癌が発生し、さらに低分化癌から未分化癌が発生した、と考えてきました。そうであれば、濾胞癌で存在する遺伝子異常は低分化癌に引き継がれ、低分化癌で存在する遺伝子異常はさらに未分化癌に引き継がれなければなりません。では、実際のデータはどうでしょうか。たしかに、すべての腫瘍に共通する遺伝子異常は存在しました。すなわち、これらの腫瘍は共通の発生母地を持つということです。ところが、濾胞癌・低分化癌・未分化癌のそれぞれが、多数の”独自の”遺伝子異常を有していたのです。すなわちこれらの腫瘍は共通の発生母地からまったく独自に進化をとげてきた、ということで1つの腫瘍から他の腫瘍へのプログレッションの形跡は認められません。これは多段階発癌を否定する動かぬ証拠です。また、濾胞癌が独自の遺伝子異常を多数有していることに注目してください。濾胞癌は年単位でゆっくりと成長するのに対して未分化癌は週単位で激しく増殖します。変異の発生頻度が増殖スピードと相関しているとすれば、濾胞癌は何年もかけてこれらの遺伝子異常を獲得したのに対して、未分化癌が変異を獲得したのはごく最近ということになります。芽細胞発癌で予想されたように、予後の良い癌が早期に増殖を開始するのに対し、悪性度の高い癌はサイレントのまま年単位で潜伏し、その後突然出てくることが分かります。
また、検証1と検証2の結果を合わせると、驚くべき事実が分かります。 患者を癌死させるような癌は中年以降でしか出てきません。またそのような癌のそもそもの発生は幼少期です。このような癌は数十年間何もせずにじっとしている、ということになります。また、この間、甲状腺に放射線を当てたりしても癌の頻度は変わらないことから”プログレッション(悪性化)”は起こっていないことが分かります。途中になんのイベントもないのに、いわば”時限爆弾”のように年数が経過することで癌が発生するのです。すなわち、甲状腺癌で将来癌死する可能性があるかどうかは5歳くらいで既に決まっています。このことから、もし、高齢型甲状腺癌の芽(癌幹細胞と言っていいかもしれません)を見つける技術が開発されれば、そのような細胞は甲状腺では経皮エタノール注入(PEIT)で簡単に消滅させることができるので、究極の予防策となることが考えられるのです。
6.過剰診断問題と福島県民健康調査の行方
芽細胞発癌説は、最近まで一部の”マニア”が知っているだけの理論でした。しかし、最近注目を集めるようになったのは、国内外において甲状腺癌の過剰診断(治療しても無駄な癌を診断してしまうこと)が問題視されるようになったからです。芽細胞発癌説は早期診断・早期治療がふさわしくないSelf-limiting
Cancerの存在を予測し、過剰診断の被害の発生を正確に予期していました。特に韓国や福島の事例では、検診を計画した専門家が芽細胞発癌の論文を読んでいたらその後の経過は違っていただろう、という研究者もいます。多段階発癌説ではすべての腫瘍はいずれ悪性化します。特に若年者で腫瘍が見つかった場合、それを長期間放置しておく、という選択肢はありません。早期診断・早期治療がすべてに優先されるのです。特に甲状腺癌は初期に転移する性質が強く、小さな癌でも転移を認めることが早期診断・治療を正当化する根拠として用いられてきました。 しかし、Self-limiting
Cancerの存在が確実視されるようになり、このような考え方は変更を求められるようになってきたのです。転移していても見つけるべきでない、治療すべきでない癌は確実に存在します。今後、多段階発癌説が構築した固定概念から脱却し、特に過剰診断、過剰治療をどう抑制するかを考えていくことが今後のがん研究の大きなテーマの一つとなるでしょう。
芽細胞発癌の理論から、今後福島で行われている甲状腺検査がどんな結果をもたらすかを予測してみましょう。これらの癌が中年以降発生する大人の癌を前倒しで診断・治療しているなら、数十年後の福島県における甲状腺癌の死亡率は低下します。しかし、芽細胞発癌説で考えれば両者は別物なので甲状腺癌の死亡率は変化しません。子供の時期に行われた手術のほどんどは無駄であった、との結論になります。また治療が必要な癌を見つけたのだとしても、若年者の小さな甲状腺癌はまだ成長期にあります。若年者に早すぎる縮小手術が行われた場合、再発率は相当高くなるであろうことが予想できます。 さらに、本当に治療しなければいけない癌は中年以降に発生します。手術で片葉切除した患者から新たな甲状腺癌が発生する、といった不幸な症例がでてしまうこともあり得るでしょう。 残念ながら、無症状の若者全員を対象とする甲状腺検診を続ける限り福島県の今後には明るい見通しは持てません。
【参考文献】
1.
Takano
T. Fetal cell carcinogenesis of the thyroid: Theory and practice. Semin Cancer
Biol 17: 233-240,
2007. Open
Access
2.
Takano T.
Fetal cell carcinogenesis of the
thyroid:A modified theory based on recent evedinces. Endocr J 61:311-320.,2014. Open
Access
3.
Takano T.
Natural history of thyroid cancer. Endocr J 64: 237-244, 2017.
Open Access
4. Takano T.Overdiagnosis
of juvenile thyroid cancer: Time to consider self-limiting cancer. (perspective)
J Adolescent Young Adult Oncol 9:286-288,
2020. Open
Access
大阪大学医学系研究科甲状腺腫瘍研究チーム:ホームへ戻る
 しかしこの考え方は根本的な問題を抱えています。”正常細胞”って何なんでしょうか。たとえば、甲状腺なら、成人で見られる甲状腺濾胞上皮細胞を指しているのでしょうか。多段階発癌を説明している教科書で、この疑問に真っ向から答えているものは実はあまり多くありません。このことを持ち出すと説明がやりにくくなるからです。すべての細胞は臓器発生初期に存在する幹細胞等の胎児性細胞から分化して産生されます。これらの胎児性細胞から癌が発生する可能性は無いのでしょうか。「ない」、と否定してしまうのははなはだ困難でしょう。しかし、可能性があるのだ、としてしまうと、次のことを考えないとなりません。、すなわち、発癌のスタートである発生母地の細胞の性質が異なるなら、その後の発癌過程も異なるであろうということです。特に、発生初期の「正常な細胞」である幹細胞等は活発に増殖しかつ癌の転移能に相当する移動能を持っています。すなわち癌細胞にそっくりな細胞です。これらの細胞から癌が発生するのであれば、従来言われていた悪性化の過程(プログレッション)は必要ありません。これらの胎児性細胞がその性質を維持したまま増殖できたらよいのでワンステップで非常に簡単に癌が発生することになります。従来の多段階発癌説ではこのようなシンプルな経路をなぜか無視して、胎児性細胞がいったん分化して癌形質を失い、先祖返りで脱分化してに癌形質を再び獲得する、という複雑な過程を経ている、としてきたのです。臓器発生初期の胎児性細胞から直接癌が発生する、これが我々が2000年の国際甲状腺学会で世界で初めて報告した芽細胞発癌説(fetal
cell carcinogenesis)の基本概念です。”正常細胞”って何だろう?という疑問に気づいてしまうと、多段階発癌説は成立させるのがもはや困難になってしまいます。多段階発癌説の創成期に活躍したBert Vogelsteinは最近、Scienceで「癌は幹細胞以外からは発生しない*」という論文を書いています(Science
355:1330-34, 2015)。おそらくこのような理論的矛盾に気づいたのだと思います。
しかしこの考え方は根本的な問題を抱えています。”正常細胞”って何なんでしょうか。たとえば、甲状腺なら、成人で見られる甲状腺濾胞上皮細胞を指しているのでしょうか。多段階発癌を説明している教科書で、この疑問に真っ向から答えているものは実はあまり多くありません。このことを持ち出すと説明がやりにくくなるからです。すべての細胞は臓器発生初期に存在する幹細胞等の胎児性細胞から分化して産生されます。これらの胎児性細胞から癌が発生する可能性は無いのでしょうか。「ない」、と否定してしまうのははなはだ困難でしょう。しかし、可能性があるのだ、としてしまうと、次のことを考えないとなりません。、すなわち、発癌のスタートである発生母地の細胞の性質が異なるなら、その後の発癌過程も異なるであろうということです。特に、発生初期の「正常な細胞」である幹細胞等は活発に増殖しかつ癌の転移能に相当する移動能を持っています。すなわち癌細胞にそっくりな細胞です。これらの細胞から癌が発生するのであれば、従来言われていた悪性化の過程(プログレッション)は必要ありません。これらの胎児性細胞がその性質を維持したまま増殖できたらよいのでワンステップで非常に簡単に癌が発生することになります。従来の多段階発癌説ではこのようなシンプルな経路をなぜか無視して、胎児性細胞がいったん分化して癌形質を失い、先祖返りで脱分化してに癌形質を再び獲得する、という複雑な過程を経ている、としてきたのです。臓器発生初期の胎児性細胞から直接癌が発生する、これが我々が2000年の国際甲状腺学会で世界で初めて報告した芽細胞発癌説(fetal
cell carcinogenesis)の基本概念です。”正常細胞”って何だろう?という疑問に気づいてしまうと、多段階発癌説は成立させるのがもはや困難になってしまいます。多段階発癌説の創成期に活躍したBert Vogelsteinは最近、Scienceで「癌は幹細胞以外からは発生しない*」という論文を書いています(Science
355:1330-34, 2015)。おそらくこのような理論的矛盾に気づいたのだと思います。 発生初期の甲状腺では3種類の胎児性細胞が確認できます。甲状腺は胎生期に舌根部で小さな細胞の塊として最初に現れます。これが
発生初期の甲状腺では3種類の胎児性細胞が確認できます。甲状腺は胎生期に舌根部で小さな細胞の塊として最初に現れます。これが
 この謎については、最近、全ゲノム・エクソーム解析のデータが出てきて何が起こっているのかようやくはっきりわかってきました。現在までに3つの論文がでていますが、いずれも同じ結果です。この図は、分化癌である濾胞癌と低分化癌、未分化癌の同一症例における共存例について全ゲノム解析でそれぞれの腫瘍の遺伝子異常を検出したものです。従来このような症例は、最初に濾胞癌があって、そこから低分化癌が発生し、さらに低分化癌から未分化癌が発生した、と考えてきました。そうであれば、濾胞癌で存在する遺伝子異常は低分化癌に引き継がれ、低分化癌で存在する遺伝子異常はさらに未分化癌に引き継がれなければなりません。では、実際のデータはどうでしょうか。たしかに、すべての腫瘍に共通する遺伝子異常は存在しました。すなわち、これらの腫瘍は共通の発生母地を持つということです。ところが、濾胞癌・低分化癌・未分化癌のそれぞれが、多数の”独自の”遺伝子異常を有していたのです。すなわちこれらの腫瘍は共通の発生母地からまったく独自に進化をとげてきた、ということで1つの腫瘍から他の腫瘍へのプログレッションの形跡は認められません。これは多段階発癌を否定する動かぬ証拠です。また、濾胞癌が独自の遺伝子異常を多数有していることに注目してください。濾胞癌は年単位でゆっくりと成長するのに対して未分化癌は週単位で激しく増殖します。変異の発生頻度が増殖スピードと相関しているとすれば、濾胞癌は何年もかけてこれらの遺伝子異常を獲得したのに対して、未分化癌が変異を獲得したのはごく最近ということになります。芽細胞発癌で予想されたように、予後の良い癌が早期に増殖を開始するのに対し、悪性度の高い癌はサイレントのまま年単位で潜伏し、その後突然出てくることが分かります。
この謎については、最近、全ゲノム・エクソーム解析のデータが出てきて何が起こっているのかようやくはっきりわかってきました。現在までに3つの論文がでていますが、いずれも同じ結果です。この図は、分化癌である濾胞癌と低分化癌、未分化癌の同一症例における共存例について全ゲノム解析でそれぞれの腫瘍の遺伝子異常を検出したものです。従来このような症例は、最初に濾胞癌があって、そこから低分化癌が発生し、さらに低分化癌から未分化癌が発生した、と考えてきました。そうであれば、濾胞癌で存在する遺伝子異常は低分化癌に引き継がれ、低分化癌で存在する遺伝子異常はさらに未分化癌に引き継がれなければなりません。では、実際のデータはどうでしょうか。たしかに、すべての腫瘍に共通する遺伝子異常は存在しました。すなわち、これらの腫瘍は共通の発生母地を持つということです。ところが、濾胞癌・低分化癌・未分化癌のそれぞれが、多数の”独自の”遺伝子異常を有していたのです。すなわちこれらの腫瘍は共通の発生母地からまったく独自に進化をとげてきた、ということで1つの腫瘍から他の腫瘍へのプログレッションの形跡は認められません。これは多段階発癌を否定する動かぬ証拠です。また、濾胞癌が独自の遺伝子異常を多数有していることに注目してください。濾胞癌は年単位でゆっくりと成長するのに対して未分化癌は週単位で激しく増殖します。変異の発生頻度が増殖スピードと相関しているとすれば、濾胞癌は何年もかけてこれらの遺伝子異常を獲得したのに対して、未分化癌が変異を獲得したのはごく最近ということになります。芽細胞発癌で予想されたように、予後の良い癌が早期に増殖を開始するのに対し、悪性度の高い癌はサイレントのまま年単位で潜伏し、その後突然出てくることが分かります。