CKDできわめて高頻度に見られる電解質異常(低Mg血症)の新たな成因
Nephrol Dial Transplant. PMID: 29796601
Proteinuria-associated renal magnesium wasting leads to hypomagnesemia: a common electrolyte abnormality in chronic kidney disease.
Oka T, Hamano T, Sakaguchi Y, Yamaguchi S, Kubota K, Senda M, Yonemoto S, Shimada K, Matsumoto A, Hashimoto N, Mori D, Monden C, Takahashi A, Obi Y, Yamamoto R, Takabatake Y, Kaimori J, Moriyama T, Horio M, Matsui I, Isaka Y.
低Mg血症は慢性腎臓病(CKD)のいかなる病期においても死亡の予測因子となることが知られています。我々は、低Mg血症がCKDの病期進行にも寄与することを糖尿病(DM)、非DMいずれにおいても過去に報告しました。このように昨今、CKDにおける低Mg血症の重要性が叫ばれてきています。しかしながら、低Mg血症は、経口での適切な治療法はおろか、その成因(特に腎内在的なもの)や、CKDにおける頻度さえ明らかになっていませんでした。
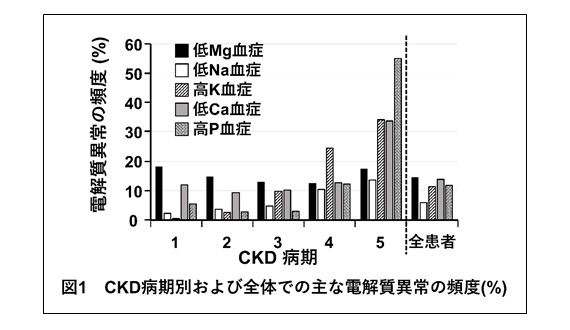
そこでまず、約5000名の外来CKD患者を対象に横断研究を行い、電解質異常(Na, K, Ca, P, Mg)の頻度を比較した結果、CKD早期(Stage1-3)に、最も高頻度にみられる電解質異常は低Mg血症であり、それは全症例を対象としても同様でした(図1)。一般的に、病期が進行するにつれ、GFR低下に伴い低Mg血症の頻度は低下すると考えられがちですが、低Mg血症の頻度は、どの病期においても15%程度で一定であり、GFRの低下したCKDでは血清Mg濃度を低下させるメカニズム(後述)が存在すると考えられました。低Mg血症を従属変数とした多変量ロジスティック回帰分析を行うと、経口Mg製剤の非使用、DMに加え、尿蛋白陽性が低Mg血症の独立した寄与因子として同定されました。
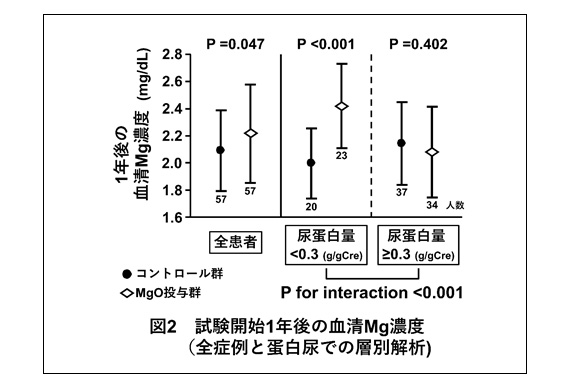
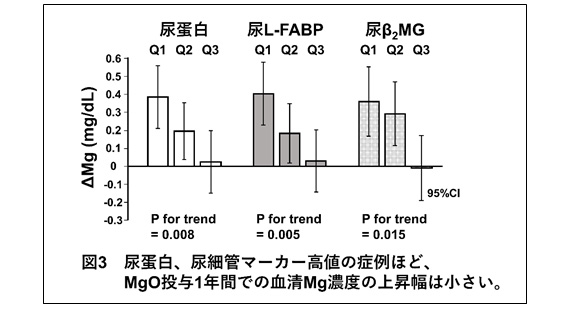
次に、CKD Stage3以降の外来患者を対象にオープンラベルランダム化比較試験を行い、酸化マグネシウム(MgO)を1年間処方された群とされていない群での1年後の血清Mg濃度を比較しました。まずは介入前のベースライン解析にて、尿蛋白や尿細管マーカー(尿β2MGと尿L-FABP)の高値は尿Mg排泄率(FEMg)の高値と有意に関連していました。媒介解析では、FEMgと尿蛋白量との関連の大部分は、尿細管マーカーを介しているとの結果を得ました。MgO投与群ではコントロール群に比して、1年後の血清Mg濃度は僅かに上昇していたものの、ベースラインの尿蛋白が0.3 g/gCre以上の症例では両群で有意差を認めませんでした。MgO群について、尿蛋白の多い症例や尿細管マーカー高値の症例では、1年間の血清Mg濃度の上昇幅は小さくなっていました。(図3)。以上の解析から、尿蛋白の多い症例では、尿細管障害を介して腎性Mg喪失が起こることで、低Mg血症が誘導されると考えられます。これが、進行したCKDで低GFRにも関わらず血清Mg濃度が低下するメカニズムの一つと考えられました。
本研究により、CKDにおける低Mg血症が極めて高頻度であること、尿蛋白による尿細管障害というありふれた病態が低Mg血症のリスクとなること、が明らかとなりました。
