リトコール酸はビタミンD受容体依存的、経細胞性経路非依存的に腸管のリン吸収を増加させる
Lithocholic acid increases intestinal phosphate and calcium absorption in a vitamin D receptor dependent but transcellular pathway independent manner.
Nobuhiro Hashimoto, Isao Matsui, Satoshi Ishizuka, Kazunori Inoue, Ayumi Matsumoto, Karin Shimada, Shota Hori, Dong Geun Lee, Seiichi Yasuda, Yusuke Katsuma, Sachio Kajimoto, Yohei Doi, Satoshi Yamaguchi, Keiichi Kubota, Tatsufumi Oka, Yusuke Sakaguchi, Yoshitsugu Takabatake, Takayuki Hamano, Yoshitaka Isaka.
高リン血症は生命予後悪化につながり、リン吸着薬による高リン血症への介入が生命予後改善を改善させることが知られています。しかし、腎臓病患者のリン代謝を適切に管理するためには、アドヒアランスの低下を引き起こすほどのリン吸着薬が必要であり、新たな視点からリン代謝を制御する方法の確立が必要な状況です。新たなリン代謝制御法確立に向け、今回我々は、リトコール酸(LCA)に注目しました。LCAは、腸内細菌により生成される二次胆汁酸であり、ビタミンD受容体 (VDR)を活性化させることが知られていました。しかし、LCAがリン代謝に与える影響は不明であり、今回検討を行いました。
野生型マウスにLCAを投与すると腸管のリン吸収が増加することが分かりました (図1)。さらに腸管上皮細胞でのみVDRが存在しないマウス (iVDRKO マウス)を作成し、このマウスにLCAを投与しても腸管のリン吸収は増加しないことが分かりました (図1)。
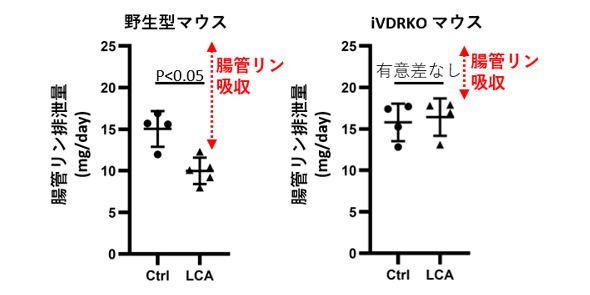
図1:LCAは腸管上皮細胞のVDRに作用し、腸管リン吸収を増加させる
また、腸内細菌が持っていて、LCAを産生させる酵素の遺伝子であるBaiE遺伝子の発現量は、便中のLCA濃度と正の相関があることもわかりました (図2)。つまり、腸内細菌はリンコントロールの新たな治療ターゲットになり得ることが示唆されました。
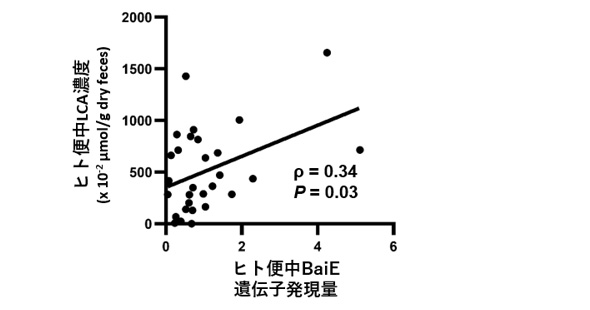
図2:腸内細菌はリンコントロールの新たな治療ターゲットになり得る
腸管のリン吸収は、Napi2bというトランスポーターにより調節されていると考えられています。しかし今回の研究では、LCAはNapi2bに影響を及ぼさないことがわかりました。LCAが腸管リン吸収を増加させるメカニズムの検討を行ったところ、Claudin3という細胞間結合を担う蛋白の腸管での発現が、LCAを投与すると低下していることが分かりました。さらには、Claudin3が存在しないCladuin3 ノックアウトマウス (Cldn3 KOマウス)では、腸管リン吸収が増加していました (図3)。
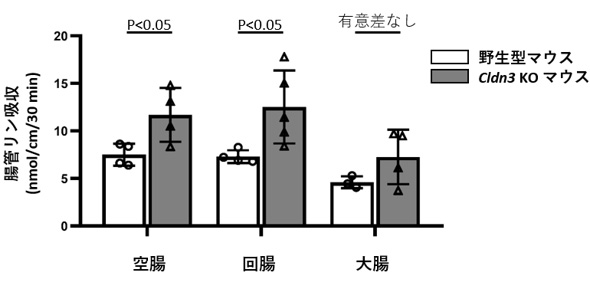
図3:Claduin3は腸管リン吸収に関わっている
本研究で、LCA、腸内細菌、Claudin3がリン代謝に関わっていることが明らかになりました。今後これらに対する介入がリンコントロールにつながるかを解明していく必要があります。
