カゼイン・卵白アルブミン・分枝鎖アミノ酸の経口摂取はリン誘導性腎尿細管間質障害を抑制する
Sci Rep. 2020 Nov 4;10(1):19038. PMID: 33149246
Dietary casein, egg albumin, and branched-chain amino acids attenuate phosphate-induced renal tubulointerstitial injury in rats.
Shimada K, Matsui I, Inoue K, Matsumoto A, Yasuda S, Katsuma Y, Sakaguchi Y, Tanaka M, Sugimoto K, Kaimori JY, Takabatake Y, Isaka Y.
高リン血症は生命予後を悪化させます。一般的に食事リン摂取量とタンパク質摂取量は正相関するため、食事タンパク質制限は食事リン制限にもなると考えられます。しかし、透析患者を対照とした臨床研究において、タンパク質(卵白アルブミン)を摂取した患者の血清リン濃度が低下する(J Ren Care. 2011;37: 16-24、Nutr Metab Cardiovasc Dis.2019; 29:45-50)、あるいはタンパク質摂取が多い者ほど生命予後が良いとする報告もあり(Am. J. Clin. Nurt.2008; 88:1511-1518)、タンパク質がリンの生体毒性に与える影響について再検討する必要がありました。
今回、我々はラットを用いてリン摂取に起因する腎障害に食餌蛋白摂取量が与える影響を検討しました。その結果、高リン(2.2%)低カゼイン(10.8%)食により生じる腎尿管間質障害が、正カゼイン(23.0%)、高カゼイン(35.2%)食によって抑制されました(図1)。タンパク源をカゼインから卵白アルブミンに変更しても、同様の結果が得られました(図2)。カゼインあるいは卵白アルブミン摂取により血漿分枝鎖アミノ酸濃度が上昇していたため、分枝鎖アミノ酸を混餌投与したところ、分枝鎖アミノ酸によってもリン負荷に起因する尿細管間質障害が抑制されました(図3)。リン負荷は腎ミトコンドリア障害を生じますが、高カゼイン、高卵白アルブミン、高分枝鎖アミノ酸給餌のいずれにおいても、腎ミトコンドリアの形態および機能が維持され、酸化ストレスが軽減しました。本研究は動物実験であり、得られた結果がヒトに外挿できるか否かは不明ですが、リン摂取と蛋白摂取の関係については、今後更なる検討が必要であることが示唆されました。
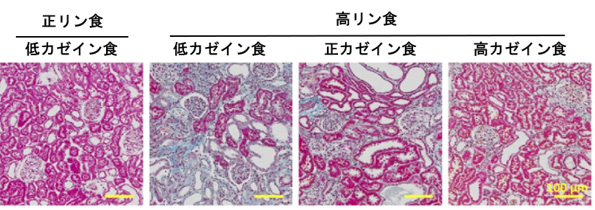
図1: 高リン食による腎尿細管間質線維化が、高カゼイン食により抑制された
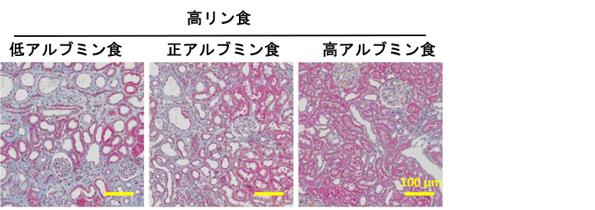
図2: 高リン食による腎尿細管間質線維化が、高卵白アルブミン食により抑制された
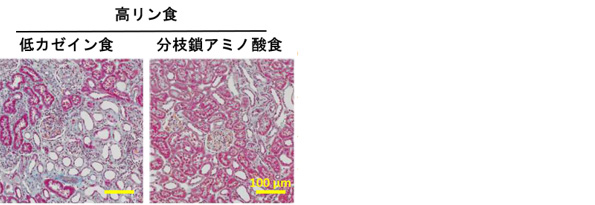
図3: 高リン食による腎尿細管間質線維化が、分枝鎖アミノ酸食により抑制された
