オートファジーによる脂肪滴分解(リポファジー)は、近位尿細管において飢餓時のエネルギー恒常性を維持する
Autophagy. 2017 Aug 16:1-19. PMID: 28813167
Lipophagy maintains energy homeostasis in the kidney proximal tubule during prolonged starvation.
Minami S, Yamamoto T, Takabatake Y, Takahashi A, Namba T, Matsuda J, Kimura T, Kaimori JY, Matsui I, Hamano T, Takeda H, Takahashi M, Izumi Y, Bamba T, Matsusaka T, Niimura F, Isaka Y.
飢餓時においては脂肪組織で分解された遊離脂肪酸が末梢組織で「脂肪滴」の形で一旦貯蔵され、必要に応じて再分解されミトコンドリアβ酸化を経て、エネルギー源となります。また腎臓、特に近位尿細管において、脂質は重要なエネルギー源であることが知られています。今回、近位尿細管において脂肪滴とオートファジーが飢餓時のエネルギー代謝に果たす役割について検討を行いました。
野生型マウスを24-48時間の飢餓状態にすると、近位尿細管の基底側に脂肪滴が観察されました。脂肪滴の一部はオートファゴソームマーカーであるLC3と共局在し、また脂肪滴分画にはLC3が豊富に存在していました。電子顕微鏡による観察で脂肪滴の一部がオートファゴソームに取り囲まれていました(図1)。
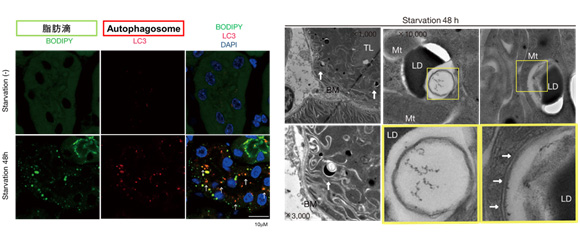
図1. 48時間飢餓下において脂肪滴の一部をオートファジーが取り囲む。
さらに近位尿細管培養細胞において、蛍光標識脂肪酸を用いたpulse chase assayから、脂肪滴がオートファゴソームによりリソソームに運ばれ分解される、“リポファジー”が存在することが明らかとなりました。またオートファジー不全近位尿細管培養細胞では、脂肪滴を適切に分解できず、脂肪蓄積、ATP低下、飢餓ストレスに対する脆弱性を認めました。同様に、近位尿細管特異的オートファジー不全マウスにおいても48時間飢餓状態とすると、野生型マウスに比し、著明な脂肪蓄積、β酸化低下を認めました(図2)。
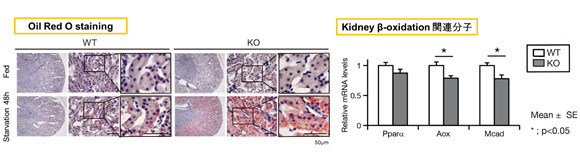
図2. 48時間飢餓下では、近位尿細管特異的オートファジー不全マウスは野生型マウスに比し、著明な脂肪蓄積、β酸化低下を認める。
以上よりリポファジーは近位尿細管において飢餓時のエネルギー恒常性維持に働くことが明らかとなりました。近年、脂肪酸代謝異常や脂肪滴の蓄積が急性腎障害や慢性腎障害の病態の進展に深く関与することが明らかとなっており、今後リポファジーによる脂肪酸代謝の制御が新たな腎臓病の治療戦略になると考えています。
