薬物モニタリングシステムの研究
【研究の概略】
口や注射により体内に入った薬は、脳や心臓をはじめとした、全身のあらゆる臓器に行き渡ります。どの臓器も、性質や役割が異なった細胞の“小さな”集団がいくつも集まってできています。病気の多くはその一部が悪くなることで起こります。薬が標的とする細胞集団に本当に届いているかどうか、そして、薬が届いた場合、その“濃度”と“細胞の働き”が時間とともにどのように移り変わっていくか、を知ることは、薬の効果や副作用を調べるうえで非常に重要です。しかし、意外にも、極めて狭い空間では、これらの指標を今までの方法で測ることができませんでした。

本研究では、これらの同時計測に、針状に加工した「ダイヤモンド電極センサ」(図1)を使った新開発の薬物モニタリングシステムにより、実験動物で成功しました。世界初のこの成果は、2017年に創刊されたNature Biomedical Engineeringへ日本のグループとして2番目に掲載されました(成果8)。本技術は、副作用を抑えて効果を最大にする投薬法や、安心・安全・有効な創薬を発展させます。本研究は、ダイヤモンド電極の作製・解析の第一人者である慶應大学理工学部の栄長泰明教授のグループと協働で進めています。

図2 微小ガラス電極センサ
【実験手法】
細胞の集団は、1ミリに満たないものも多くあります。私たちが中心となり新たに開発した薬物モニタリングシステムは、2つのセンサーから成ります。1つは、先のサイズが1ミリの25分の1(40マイクロメートル)である「針状ダイヤモンド電極センサ」(図1)であり、これで薬の濃度を敏感に測ります。ダイヤモンドを使った理由は、この素材が一般的な電極材料である炭素・金・白金などに比べて、(1)多くの種類の化合物が測定できる、(2)反応が素速く安定である、(3)ノイズが少ない、などだからです。もう1つの「微小ガラス電極センサ」(図2)は、先が1ミリの1,000分の1(1 マイクロメートル)で、細胞の電気信号を直接観察することができます。病院や薬局で処方される薬の約15%は、この電気信号を特定の臓器で強めたり弱めたりします。
これら2つのセンサを、目的とする細胞集団の近くに入れることにより、刻々と変わる薬の振る舞いと細胞の活動を“同時にリアルタイムで”モニタリングすることに成功しました。 図3は、抗てんかん薬ラモトリギンをラットに静脈注射した際の“脳”での反応です。右パネルが実験結果です。ラモトリギンの濃度(ピンク)が上がりはじめると同時に、神経細胞の電気活動(赤)が強く抑えられています。その後、薬はゆっくり推移し、投与後15分ほどで減少に転じていくこともわかります。
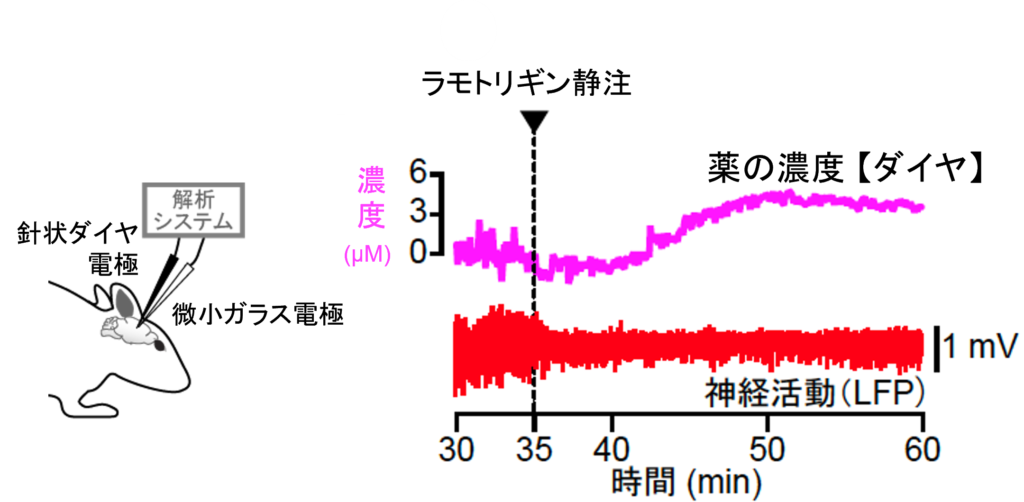

図4は、高血圧の治療に使われる利尿薬ブメタニドをモルモットに与えた際の“内耳”での反応です。内耳は鼓膜(こまく)の奥にあり、音を電気信号へ変えて脳へと運ぶ小さなカタツムリ型の臓器です(図4左)。ブメタニドは、時に内耳蝸牛の血管条と呼ばれる細胞シート層に備った生体電池を悪くして難聴を起こします。右パネルが測定結果です。ブメタニドを静脈注射すると、この薬の濃度(緑)が急に上がり、投与後1分余りですぐに下がっていくのがわかります。同時に測った生体電池の起電力(赤:内リンパ液の電位)は、ブメタニドの濃度がピークになったころから低下していきます。また、薬の変化の様子は、図3と図4で明らかに違います。
抗がん剤ドキソルビシンの振る舞いも、モルモットの体内で測ることができました。さらに、この薬物モニタリングシステムは、さまざまな抗がん薬、抗うつ薬、抗菌薬の計測にも使える可能性があることもわかりました。工夫をすれば、心臓や腎臓などでも測定できると考えています。したがって、汎用性の高い技術です。
【本研究の展開】
本研究で開発した技術を活用・応用すれば、以下のような波及効果が見込まれます。
(1)安心・安全・有効な創薬の発展。
(2)副作用をできるだけ抑え、薬効を最大にする薬の投与法の考案。
(3)ドラックリポジショニング(註1)の推進。
(註1)特定の病気に効く既存薬から、別の病気に効く薬を見つけだすこと。 (4)オーダーメイド治療法の展開。
個人個人に観察される薬効や副作用の差は、DNAマイクロチップをはじめとした技術により、SNPsなどによって徐々に説明されるようになってきています。また、薬を標的の細胞のかたまりにピンポイントで届かせようとするドラックデリバリーシステムに関しても、数多くの優れた研究が進行しています。しかし、様々な局面において、実際に生体内の局所でいかに薬物が振る舞い、いかに薬の効きめが推移していくかは、まだまだブラックボックスです。わたしたちの薬物モニタリングシステムは、その溝を埋める技術となるかもしれません。
また、ダイヤモンド電極センサをさらに加工・改良すれば、重症の患者さまに埋め込んで薬物濃度を24時間モニタリングするシステムや、臨床においてその場ですぐに薬物濃度を測定できるポータプルシステムの創成も可能です。いわゆるPoint-of-CareによるTherapeutic Drug Monitoringを実現し、次世代の医学・医療の発展に少しでも寄与できるように研究を進めていきます。
この研究に関する主な成果
(1)Sun S, Itagaki S, Nishi R, Shan X, Ogata G, Yamamoto Y, Einaga Y, Hibino H, Chen Z, Shiigi H (2026). Development of Magnetic Microbeads Equipped with Temperature-Responsive Artificial Antibodies for Efficient Anticancer Drug Administration. Anal Chem, in press.
(2)Ahmad NB, Sawamura S, Ogata G, Ota T, Tokudome K, Moriyama H, Tanaka I, Ikarashi K, Takai M, Kita S, Furutani K, Kusuhara H, Einaga Y, Hibino H (2026). Real-time detection of cardiotoxic anticancer drug by diamond microsensor in the skin and combined monitoring of electrocardiogram in live rats. ACS sensors 11:892-908.
(3) Zhou S, Chino Y, Kasama T, Miyake R, Mitsuzawa S, Luan Y, Ahmad NB, Hibino H, Takai M (2024). Biocompatible core-shell microneedle sensor filled with zwitterionic polymer hydrogel for rapid continuous transdermal monitoring. ACS Nano,18(39):26541–26559.
(4) Hibino H (2024). Toward Interdisciplinary Collaboration between Electrochemistry and Physiology: Status Quo, Challenges, and Prospects. Electrochemistry 92(2):022002. doi: 10.5796/electrochemistry.23-68115
(5)Saiki T, Ogata G, Sawamura S, Asai K, Razvina O, Watanabe K, Kato R, Zhang Q, Akiyama K, Madhurantakam S, Ahmad NB, Ino D, Nashimoto H, Matsumoto Y, Moriyama M, Horii A, Kondo C, Ochiai R, Kusuhara H, Saijo Y, Einaga Y, Hibino H(2023). Heliyon 9(5):e15963.
(6) Moriyama H, Ogata G, Nashimoto H, Sawamura S, Furukawa Y, Hibino H, Kusuhara H, Einaga Y (2022). A rapid and simple electrochemical detection of the free drug concentration in human serum using boron-doped diamond electrodes. Analyst, 147:4442-4449.
(7) Sawamura S, Ogata G, Asai K, Razvina O, Ota T, Zhang Q, Madhurantakam S, Ino D, Kanzaki S, Saiki T, Matsumoto Y, Moriyama M, Saijo Y, Horii A, Einaga Y, Hibino H (2021). Analysis of Pharmacokinetics in the Cochlea of the Inner Ear. Frontiers in Pharmacology 12:633505.
(8) Hanawa A*, Ogata G*, Sawamura S, Asai K, Kanzaki S, Hibino H#, Einaga Y#. In vivo real-time simultaneous examination of drug kinetics at two separate locations using boron doped diamond microelectrodes. Anal Chem, (2020), 92(20), 13742-13749[*: equal contributors][#: corresponding authors].
(9) Uen T, Kushiro K, Hibino H, Takai M. Surface functionalization of carbon-based sensors with biocompatible polymer to enable electrochemical measurement in protein-rich environment. Sens Actuators B Chem,(2020), 309, 127758.
(10) Asai K,Yamamoto T, Nagashima S, Ogata G, Hibino H, Einaga Y*. Electrochemical aptamer‐based sensor prepared by utilizing strong interaction between DNA aptamer and diamond. Analyst,(2019), doi: 10.1039/c9an01976f. [*: corresponding author]
(11) Hanawa A, Asai K, Ogata G, Hibino H, Einaga Y. Electrochemical measurement of lamotrigine using boron-doped diamond electrodes. Electrochimica Acta, (2018), 271: 35-40.
(12) Ogata G, Ishii Y, Asai K, Sano Y, Nin F, Yoshida T, Higuchi T, Sawamura S, Ota T, Hori K, Maeda K, Komune S, Doi K, Takai M, Findlay I, Kusuhara H, Einaga Y, Hibino H. A microsensing system for the in vivo real-time detection of local drug kinetics. Nature Biomedical Engineering, (2017), 1: 654-666.
この研究に関する主な記事
(1) Alan D (2018). In vitro veritas: Biosensors and microarrays come to life. Science 359:1287-1290.
(2) MONOist医療技術ニュース(2017/09/01).『薬の濃度・効果を生きた動物の脳や内耳からリアルタイムに計測するセンサー』
(3) 製薬業界の転職支援アンサーズ (2017/08/18). 『新潟大と慶應大と東大、世界初!薬の挙動と作用のリアルタイム計測に成功』
(4) fabcross for エンジニア (2017/08/18). 『新潟大や慶大など、薬の振る舞いと効き目を体内で測る新技術を開発』
(5) 新潟日報 (2017/08/17). 『薬の作用、針状センサーで即時計測新潟大大学院・日比野教授らのグループが開発』
(6) マイナビニュース (2017/08/16). 『針状ダイヤモンド電極センサーで、薬の振る舞いと効きめを体内測定-新潟大』
(7) 日本経済新聞 (2017/08/13). 『新潟大など、動物体内の薬濃度と細胞を観察』
(8) J-CASTニュース (2017/08/12). 『薬の効き目がすぐわかる画期的センサー 新潟・慶応・東京大チームが世界初の開発』
(9) 日刊工業新聞 (2017/08/10). 『新潟大など、薬剤の振る舞いと作用を同時計測するシステム開発』
(10) 日本経済新聞 (2017/08/10). 『新潟大と慶大と東大、針状に加工した「ダイヤモンド電極センサー」を使用した薬物モニターシステムを開発』
(11) Yahoo ニュース(時事通信)(2017/08/10). 『薬の効き目、体内で測定=特殊センサーで即時把握―新潟大など』






