RESEARCH
神経遺伝子学教室は、RNA生物学をテーマにした遺伝子機能制御学教室と、神経細胞医科学教室が融合し、2014年4月に発足しました。2016年4月には情報解析室も整備し、情報系専任教員も着任したことで、ウェット、ドライを含めて、RNA研究、疾患病態研究をシームレスに行う体制が構築され、現在に至っています。当教室では主に以下のようなテーマに関する研究を行っています。
- RNA結合タンパク質やnon-coding RNAの機能解明を目指したRNA生物学(河原、中濱)
- 筋萎縮性側索硬化症(ALS)などの神経変性疾患の病態解明と治療法の確立(河原、渋谷)
- 生命の「設計図」をデータで読み解く — データ駆動型オミクス情報解析(加藤)
- 転写因子MRTFsによる細胞骨格維持機構とその破綻がもたらす疾患研究(村井)
RNA結合タンパク質やnon-coding RNAの機能解明を目指したRNA生物学(河原、中濱)
Abstract
難病を解明するためには、様々な分野の最新の知識と技術を取り入れ、広い視野を持って対処する必要があります。当教室では、RNA代謝を切り口に疾患病態を解明する「RNA病態学」という新しい研究領域の創造と発展を目指します。そのために、RNA biologyの基礎研究に力を入れています。ヒトゲノムDNAの約80%の領域からRNAは転写されており、そのほとんどはタンパク質をコードしないnon-coding RNAです。これらは、単に「受動的発現」をしているのではなく、転写や蛋白質発現を制御する「能動的機能」を持つことが解明されてきましたが、まだ未解決な謎が多く残されています。また、これらを制御するRNA結合タンパク質も、ヒトには1,000個以上あることが最近の研究で明らかとなってきましたが、そのほとんどは機能未知です。つまり、この領域には難病を解き明かすための多くの手がかりが隠されていると予想されます。私たちの研究室では、研究対象とするRNA、RNAの修飾や機能、RNA結合タンパク質、疾患を特に制限していません。現在行っている研究は、RNA biologyの基礎研究から、microRNAを用いた疾患スクリーニング法の開発と言った応用研究まで多岐・多彩です。対象疾患も、神経疾患、循環器疾患、婦人科系疾患、自己免疫疾患など多様です。中でも、近年、RNA修飾はエピトランスクリプトームと呼ばれる研究分野として確立しつつあり、私たちは、特にRNA編集という転写後修飾の研究分野で世界を牽引しています。
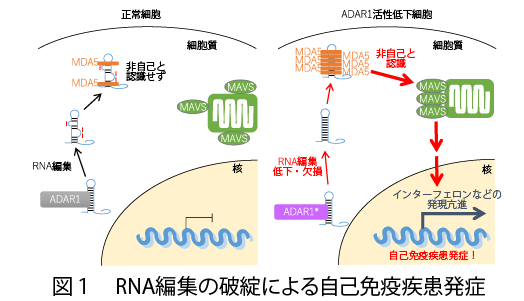
2本鎖RNA中のアデノシンをイノシンへと置換するRNA編集は、哺乳類において最も普遍的に生じているRNA修飾であり、転写後にADARによって触媒されます (図1)。99%以上は非コード領域、非コードRNAに生じていますが、近年これがRNAの自己化に必須の修飾であることが判明しつつあります。このため、RNA編集の破綻は、自己免疫疾患発症へとつながります (図1)。現在、私たちは、自己免疫疾患を誘発する鍵を握るRNA編集部位の同定を進めています。
Welcome message
難しいからこそ難病の解明に挑んでみたいと思う意欲的な方はいつでも歓迎します。
Related publications
Tuangton et al., J Immunol, 2020; Costa et al., RNA, 2020; Nakahama et al., EMBO Rep, 2018; Oshima et al., Chem Commun, 2018; Miyake et al., Cell Rep, 2016; Matsumoto et al., Circ Res, 2013; Kawahara et al., Nat Protocols, 2012; Kawahara et al., Science, 2007など
筋萎縮性側索硬化症(ALS)などの神経変性疾患の病態解明と治療法の確立(河原、渋谷)
Abstract
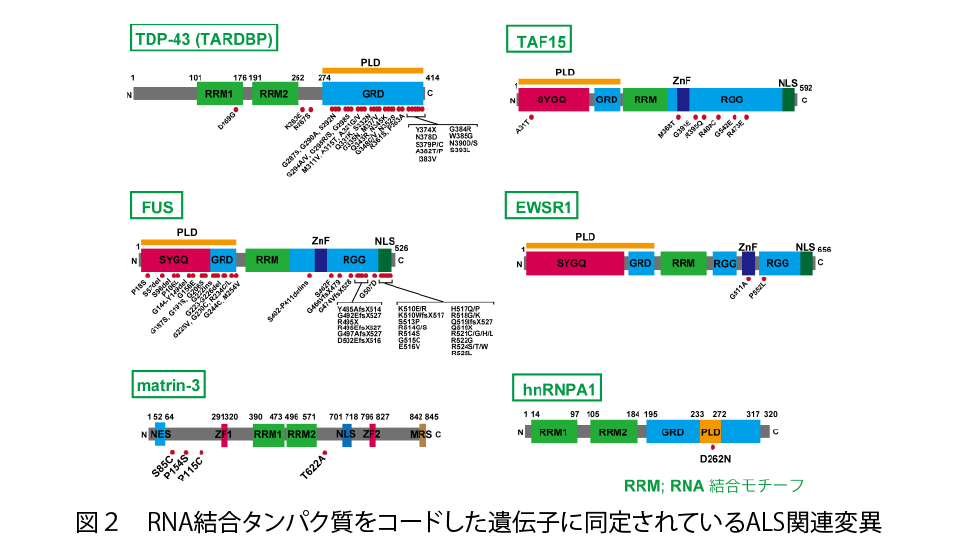
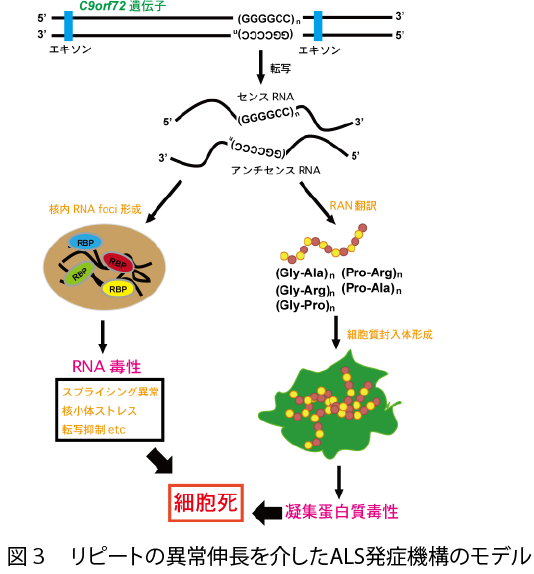
河原はこれまで神経内科医として、アルツハイマー病、パーキンソン病、筋萎縮性側索硬化症 (ALS)、脊髄小脳変性症など多くの神経難病と闘う患者さんと接してきました。現在も、限られた時間の範囲内ではありますが、患者さんの診療を継続しており、自らの研究の方向性を決定付けています。中でも、ALSの病態解明と治療法の確立は、教室のライフワークとなっています。ALSは、運動神経細胞が選択的に脱落し、多くの場合、全身の筋力が数年で失われてしまう難病です。日本には9,000人弱の患者さんがいますが、9割に遺伝性がなく、河原が研究をはじめた頃には限られた情報しかありませんでした。しかし近年の研究技術の飛躍的な発展に伴い多くの知見が得られるに至っています。例えば、 TDP-43やFUSといったRNA結合タンパク質をコードした遺伝子に、しばしばALSと関連した変異が見つかるようになったこと (図2)や、C9orf72遺伝子のイントロン中にあるGGGGCCリピート配列の異常伸長が一部のALSの原因として発見されたことが挙げられます (図3)。これらの知見は、ALSの病態の根底にRNA代謝異常があることを示唆しています。また、これら複数の遺伝子変異が、ALSだけでなく、認知症を主症状とする前頭側頭葉変性症 (FTLD)の原因ともなることが分かってきています。これは、変性しやすい神経細胞の特徴を探る上で極めて重要な手がかりとなります。過去10年間に得られた知見の量と質を鑑みると、今後10年の間にALSの根本的な原因が解明され、治療法の道筋が立てられるかもしれません。そのためにも、従来の既成概念やアプローチ法を打破する必要性があると考えます。
Welcome message
現在、私たちは、新たなALSのモデルマウスを作製し、発症メカニズムの研究を行っています。また、製薬会社と共同で、治療法の開発に取り組んでいます。難病を解明し、治療法へ結びつけるチャンスは以前にもまして高まっています。難しいからこそ難病の解明に挑んでみたいと思う意欲的な方はいつでも歓迎します。
Related publications
Uemura et al., Genes to Cells, 2018; Li et al., Nat Commun, 2015; Yokoshi et al., Mol Cell, 2014; Kawahara et al., PNAS, 2012; Kawahara et al., Nature, 2004など
Related websites
生命の「設計図」をデータで読み解く — データ駆動型オミクス情報解析(加藤)
Abstract
遺伝子は、生命の運命を分子レベルで左右する因子の一つです。近年、ハイスループットシークエンシングをはじめとする実験技術の急速な普及により、遺伝子配列を網羅的・大規模に読み取ることが可能となり、「全体像から特定の生命現象を理解する」トップダウン型のアプローチが現実のものとなりました。
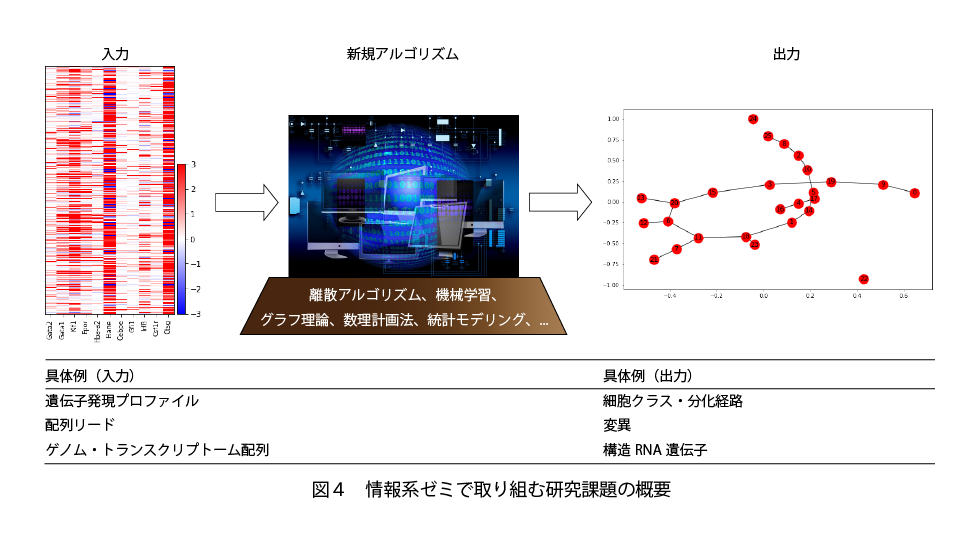
しかし、これだけ大量のデータが得られるようになると、新たな問いが生まれます。ノイズに埋もれた膨大なデータの中から、本当に意味のある情報をどう取り出すか? — これが、当教室バイオインフォマティクスゼミに共通する中心テーマです (図4)。
その答えを追い求めるために、情報科学・数理科学の洗練された理論に裏打ちされた新規アルゴリズムの開発に取り組んでいます。既存ツールをそのまま使うだけでなく、「自分たちで手法を作る」 ことを重視している点は、医学部の研究室としては異色の強みです。
もちろん、アルゴリズムを作るだけでは「絵に描いた餅」。当研究室はウェット実験にも力を入れており、マウスなどのモデル生物から得られる実データ(遺伝子発現情報など)を活用できる環境が整っています。自分が開発した手法を、本物のデータで検証し、生物学的な発見につなげる — このサイクルを一貫して経験できることが、本ゼミ最大の魅力です。
Details
- 細胞を「一つひとつ」見る — シングルセルデータによる細胞分類・動態予測
- 細胞をどう「分類」するか? — 細胞集団の中には、従来の方法では気づかれない希少なサブタイプが潜んでいます。そうしたrare cell subtypeを発見するクラスタリングと、細胞が時間とともにどのように変化していくかを「疑似時間」として推定する細胞分化経路の解析は、当ゼミが取り組む中心課題の一つです。当教室では、分岐を持つ2つのデータセット間で細胞経路を効率よく比較できるツール CAPITAL を開発しました(video abstract も以下で公開中)。
- 「スナップショット」の限界を超える — シングルセルデータはある瞬間の細胞の姿を切り取ったものに過ぎず、時間の流れや組織内での位置情報は失われています。映画の一コマから物語全体を読み解くような難しさがそこにはあります。当教室では現在、この限界に正面から挑み、時空間情報を統合した新しい解析手法の開発を進めています。細胞がいつ・どこで・何をしているのかを同時に捉えることで、これまで見えなかった細胞集団の機能解明を目指しています。
- 配列リード直接比較によるゲノム構造変異解析
- RNA高次構造予測のためのゲノム・トランスクリプトームワイド解析
生命を構成する最小単位は細胞です。しかし、従来の解析では細胞集団を「平均」として捉えるしかなく、個々の細胞の顔は見えていませんでした。シングルセルRNA-seqの登場により、一つひとつの細胞の遺伝子発現を直接読み取ることが可能となり、これまで群衆に埋もれていた細胞の個性を捉えられるようになりました。
この技術がもたらす問いは、大きく二つあります。
体細胞のゲノム配列上に生じる1塩基置換やインデル(挿入欠失)などの変異はがんの発生や進行に関係すると言われています。また、ゲノム編集では、標的配列以外の領域に変異が入るオフターゲット効果が懸念されています。これらの問題は、ハイスループットシークエンサーから得られる配列リードを比較し、変異を検出することで対応可能です。当教室では、コントロールおよび条件由来リード群を従来より少ないメモリ使用量で直接比較するツールBivartectを開発しました。ここで、Bivartectは他のゲノムマッピングに基づく手法に比べて、ゲノム編集におけるオフターゲット候補が劇的に絞り込めることを実証しました。
ヒトゲノムの大多数がRNAに転写されることが分かっているのですが、その機能が未知のものが多く、RNA機能解析はヒトを理解する上で取り組まなければならない重要な課題の1つです。機能と構造には相関関係があり、構造解析を切り口としてRNAの機能解明に迫るアプローチが広く行われています。また、「ヒトとは何か?」という問いに答えるためには、他の生物との比較が重要な手掛かりを与えると期待されます。これまで、2生物間の比較ゲノム解析で構造RNA遺伝子を検出するツールDotcodeRを開発しました。現在、より特殊な構造(G4重鎖など)がなぜ形成されるのか、それが進化的に生物種間でどう保存されているのかという観点から、アルゴリズム開発を行っています。
Welcome message
- 情報学は方法論の学問 —「解けた」ではなく「なぜ解けるか」を大切にします
- 理論と実装、どちらも本物 — サイエンスとエンジニアリングの融合を体現します
- 医学部から理工学の最前線へ — 境界を越える学びがここにあります
- 医学×情報×工学の交差点で、「作れる医師」になってください
Related publications
Sugihara et al., Nature Communications, 2022; Shimmura et al., Bioinformatics, 2020; Kato et al., BMC Genomics, 2017; Kato et al., Bioinformatics, 2017; Kato et al., Nucleic Acids Res, 2012など
転写因子MRTFsによる細胞骨格維持機構とその破綻がもたらす疾患研究(村井)
Abstract
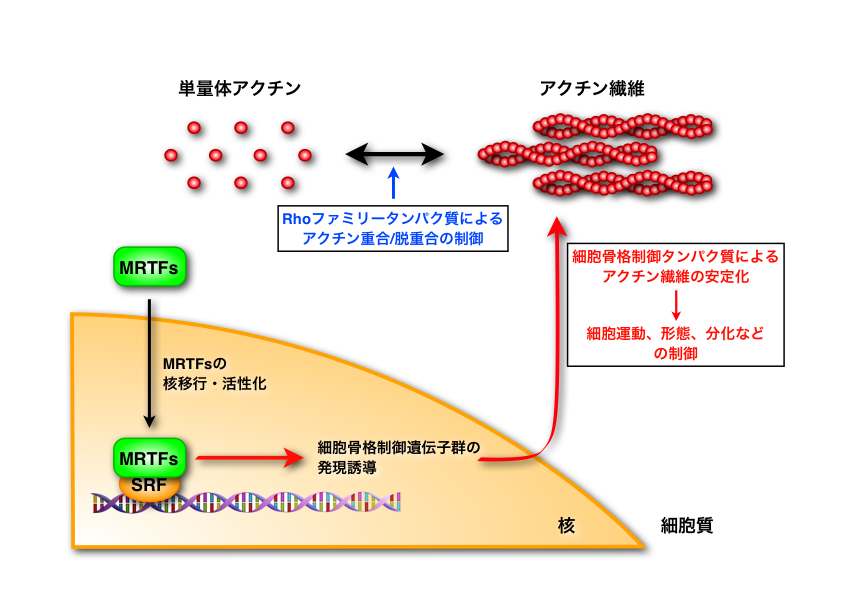
アクチンは筋組織において筋収縮を司る主要なタンパク質ですが、非筋肉細胞においても豊富に存在し細胞の動的なイベントを制御する基本的な構造タンパク質です。アクチンタンパク質の多くは細胞内で重合し繊維状の構造体として存在しますが、このアクチンの重合・脱重に加えてモータータンパク質であるミオシンとの協調的な作用が細胞運動や細胞内の物質輸送に必要な推進力を生み出しています。このようなアクチンの機能を制御する分子として低分子Gタンパク質であるRhoファミリータンパク質が良く知られています。Rhoファミリータンパク質は細胞外からの刺激に応答して速やかに活性化され、アクチンの重合・脱重合やミオシン機能を制御しています。このような速やかで一過的な応答に対し、細胞の分化やガン化の過程ではアクチン細胞骨格の恒常的な再編成が行われており、Rhoファミリーによる一過的な制御とは別の機構が存在するのではないかと考えられていました。私たちは転写因子であるmyocardin-related transcription factors (MRTFs)が数多くの細胞骨格関連遺伝子の発現を同時に制御することでアクチン細胞骨格の再編成を引き起こすことを明らかにしてきました。現在、50以上の細胞骨格関連遺伝子がMRTFsによる発現制御を受けていることが知られていますが、MRTFsはこのような包括的な発現制御を介して実に多様な生理現象に関与しています。近年、肝硬変、間質性肺炎などの線維化疾患や心疾患、ガン、動脈硬化、統合失調症などの病態にもMRTFsが深く関与していることが報告され、これら疾患の治療ターゲット分子としても注目を集めています。私たちは、特にMRTFsの寄与度が特に高いと思われるガン細胞の転移や組織の線維化の過程に注目し、MRTFsの活性制御機構の解明やMRTFs特異的な阻害剤の開発に取り組んでいます。本研究が上記疾患の発症メカニズムの解明や治療薬の開発につながるものと期待しています。
