|
私は大学院を修了した後、1998年よりドイツに留学しました。大学院生として私に与えられた研究テーマは、中枢神経の再生とは関係のないものでした。留学先で私に与えられた研究テーマは、p75という神経細胞に発現している受容体の機能を明らかにするということでした。私はいつの日か再生というテーマに取り組みたいと考えていましたが、実験自体が好きだったので、どのようなテーマでもそれなりに楽しいと思って日々を過ごしていました。
当時、p75は細胞死を引き起こす受容体だと考えられていました。p75から細胞死に至るシグナル伝達機構は何だろうかという疑問を解き明かすために、私は分子生物学の手法を使って、ニワトリのすべての遺伝子からp75に結合する分子を探索するという実験を行っていました。結合する分子を手繰っていくことで、その分子がどのような連鎖反応を起こしているかがわかるのです。
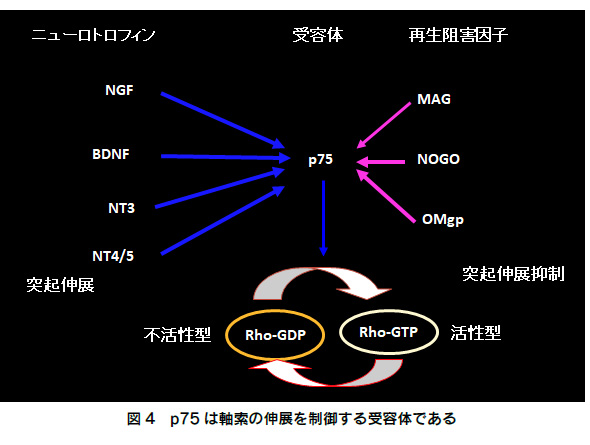
実験を進めていくと、意外なことにRhoというタンパク質が釣り上げられてきました。Rhoは細胞死を引き起こすという機能もないわけではなかったのですが、主としてアクチン骨格系、あるいはチューブリンを制御することによって、細胞の形をつくる因子として知られていました。私は、一連の実験によってp75は神経細胞の軸索の伸展を制御するタンパク質であることを明らかにしました。p75はRhoを不活性化することで、そのような効果を惹起していたのです(図4)。つまり、p75はとくに発生期の神経細胞に発現していて、Rhoを不活性化することで軸索を伸ばし、神経のネットワークを形成するのに役立っていたのでした。p75を持たないマウスは、このネットワークの形成がうまく行われていなかったのです。私の研究テーマは細胞死のシグナルという当初の予測から外れて、思わぬp75の機能を探り当てることになりました。
この成果を論文に発表した後に、私はドイツから帰国して、以前に大学院生活を送らせていただいた大阪大学で研究を続ける機会を得ることができました。この頃には、中枢神経の再生という長年心に秘めていたテーマに取り組みたいと意識し始めていました。私の論文が出た後に、さまざまな神経細胞で軸索の伸展を制御するキーとなる因子がRhoであることが示されつつあり、「Rhoの活性化を制御するp75が軸索再生阻害因子の受容体ではないのだろうか?」と思うに至ったのです。
このような大胆な予測や仮説は、通常はめったに当たることはないでしょう。なぜなら、もし仮説通りだとすると、p75はRhoを活性化できるだけでなく、不活性化もできるという、二面性を持った複雑な受容体だということになるからです。しかしこのときは、予測通りに実験が進んでいきました。私は、p75がこの再生阻害タンパク質の受容体であり、このp75により神経細胞のなかでRhoが活性化されることで、軸索の伸展が止まることを突き止めたのです(図4)。
実験を始めて半年後には論文にまとめることができましたが、p75が、発生期には軸索を伸展させ、成体ではそれを抑制するというコンセプトはなかなか受け入れられず、論文を投稿しても厳しい評価を受けて落ち続けました。しかし、2002年に論文でようやくその成果を発表できた後には、外国の研究者から祝福の言葉をもらったり、米国の科学雑誌のインタビューが舞い込んだりするようになりました。多くの追試によって私の実験結果が正しかったことが確認されたのです。そして3年後の2005年に、神経再生の分野の研究者に与えられる米国のアメリテック賞を、日本人としては初めて受賞することになったのでした。
|


