長谷川 哲雄、石井 優 ≪免疫細胞生物学≫ 関節炎で骨を破壊する“悪玉破骨細胞”を発見
2019年11月19日
掲載誌 Nature Immunology
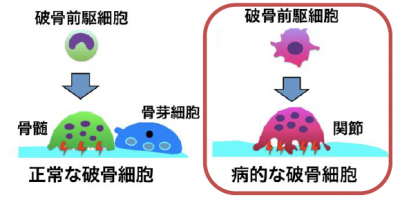 図1:悪玉破骨細胞の同定
図1:悪玉破骨細胞の同定
異常に活性化し、骨を破壊する病的な破骨細胞(悪玉破骨細胞)を同定し、正常な破骨細胞とは性質も起源もことなることを明らかにした。 クリックで拡大表示します
研究成果のポイント
- 炎症関節の細胞を採取・解析する技術を独自に開発し、関節炎で病的に骨を破壊する“悪玉破骨細胞”を同定した。
- “悪玉破骨細胞”は、通常の骨代謝を担う“善玉破骨細胞”とは、性質も起源も異なることが分かった。
- “悪玉破骨細胞”のみを特異的に阻害することで、善玉の破骨細胞が担う正常な骨の新陳代謝には影響を与えずに、関節リウマチ患者の病的な骨破壊のみ完全に阻止する画期的な治療薬開発が期待される。
概要
大阪大学 大学院医学系研究科の長谷川哲雄 特任研究員、石井優 教授(免疫細胞生物学)らの研究グループは、破骨細胞には正常な破骨細胞とは性質も起源も異なる”悪玉破骨細胞“が存在することを世界で初めて明らかにしました。
破骨細胞は、古く傷んだ骨を壊し、その後に骨芽細胞による骨新生を促すことで骨の健康さ(新陳代謝)を維持するという「良い働き」をします。その一方で、関節リウマチやがんの骨転移といった病気では、この破骨細胞が異常に活性化することで骨の破壊を起こすという「悪い働き」をしてしまうことが知られています。これまでの通説では、この破骨細胞は一種類であり、働き方が異なることで、「良い働き」や「悪い働き」を行うと考えられてきましたが、今回、石井優 教授らの研究グループは、これらの細胞は元々異なるものであり、病的な骨破壊を行うための“悪玉破骨細胞”が存在することを同定しました(図1)。
関節炎を発症させたマウスの関節組織から細胞を回収し解析する独自の方法を確立させることで、炎症関節組織には、病的に骨を破壊する“悪玉破骨細胞”へと変化する特殊なマクロファージ(悪玉破骨前駆細胞)が存在することを突き詰め、これを “arthritis-associated osteoclastogenic macrophage; AtoM(アトム)” と命名しました。さらに、AtoMができるときに必要な分子を同定し、これを抑制することで、AtoMや、そこから生じる“悪玉破骨細胞”が特異的に阻害され、骨の破壊を強力に抑えることを証明しました。今後、関節リウマチ患者の病的な“悪玉破骨細胞”を標的とした新たな治療薬開発が期待されます。
本研究成果は、英国科学誌「Nature Immunology」に、11月19日に公開されました。
研究の背景
古い骨を溶かす“破骨細胞”は、生理的な状態では骨の内側のみに存在し、骨を造る“骨芽細胞”と協調して骨構造を緻密に維持しています。一方、この“破骨細胞”は関節リウマチなどの病的な状態では関節組織に発生し、骨を“外側”から壊すことで関節構造を破壊します。
これまでに“破骨細胞”とその“前駆細胞”の研究は、骨髄や脾臓や血液の細胞を用いて数多く行われてきましたが、実際に病的な骨破壊が起こる“関節組織”を用いた解析は、病変部位が非常に小さいため詳細に行われてきませんでした。これにより、正常な破骨細胞の発生過程と病的な破骨細胞の発生過程が同じなのか、明らかではありませんでした。
本研究の成果
石井教授らの研究グループでは、関節炎において病的な骨破壊が起こる部位の組織(関節組織と骨の境界領域)を単離する独自のプロトコールを開発しました(図2)。これにより、関節炎を発症した関節組織には、正常な骨の中には存在しない病的な“破骨前駆細胞”が存在することが明らかになり、「arthritis-associated osteoclastogenic macrophage (AtoM)」と命名しました(図3)。AtoMは、関節に常在している細胞からではなく、骨髄由来の細胞が血流を介して関節に流入した後にM-CSF※1に反応して発生し、うち約10%の細胞が関節局所で病的な“破骨細胞”へと分化していくことがシングルセル解析※2を用いて明らかになりました。また、生理的な破骨細胞へ分化するために必要なRANKL(ランクル)※3に加え、炎症性サイトカインであるTNF※4を同時に投与するとさらに破骨細胞へ分化する能力が高まることが明らかになりました。
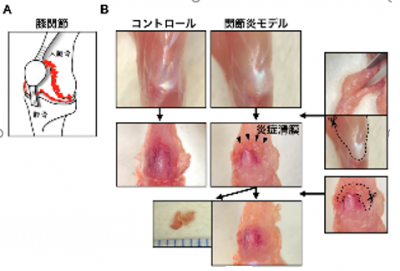 図2: 関節組織の単離プロトコールの開発
図2: 関節組織の単離プロトコールの開発
クリックで拡大表示します
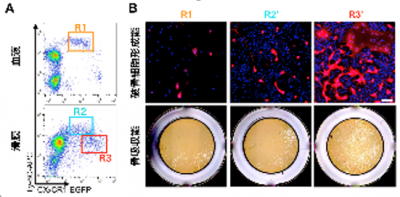 図3:関節組織の破骨前駆細胞の同定
図3:関節組織の破骨前駆細胞の同定
A.関節のみにR3の細胞集団が存在する B.関節のR3の細胞集団は著明な破骨細胞形成能力と骨を溶かす能力を有す クリックで拡大表示します
さらに網羅的な遺伝子発現を調べることで、AtoMがFoxM1と呼ばれる転写因子により部分的に制御されていることが示され、FoxM1の阻害薬がマウスモデルにおいても、関節リウマチ患者さんの関節液から採取した細胞においても、破骨細胞への分化を阻害することが明らかとなりました(図4)。
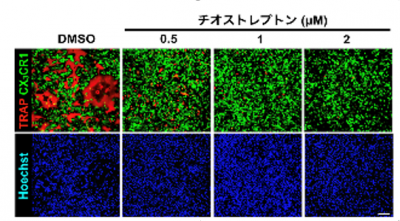 図4:FoxM1阻害薬がAtoMの破骨細胞分化を阻害する
図4:FoxM1阻害薬がAtoMの破骨細胞分化を阻害する
クリックで拡大表示します
本研究成果が社会に与える影響(本研究成果の意義)
関節リウマチは、全人口の約1%が罹患する、自己免疫疾患の中で最も頻度の高い病気の一つです。本疾患や、慢性的な関節炎を惹起する疾患群は、最終的に関節の表面に形成される病的な破骨細胞が骨を破壊することで著しい身体機能の低下、ひいては生命予後の悪化を招きます。本研究成果により、病的な破骨細胞が発生する過程が詳細に解き明かされたことで、関節の表面に形成される病的な破骨細胞をターゲットとする新たな治療法の開発が期待されます。
用語説明
※1 M-CSF(macrophage colony stimulating factor)
単球系細胞が破骨細胞へ分化するために必須のサイトカインの一つであり、単球系細胞の増殖や分化に関与する。
※2 シングルセル解析(single-cell RNA sequencing)
一つの細胞に含まれるメッセンジャーRNAからcDNAを作成し、増幅した後に次世代シークエンサーを用いて読み取ることで、全遺伝子の発現量を細胞毎に定量解析する手法。
※3 RANKL(ランクル:receptor activator of nuclear factor-kappa B ligand)
単球系細胞が破骨細胞へ分化するために必須のサイトカインの一つであり、抗RANKL抗体はヒトにおいて骨粗鬆症や関節リウマチの治療薬として用いられている。
※4 TNF(tumor necrosis factor)
主にマクロファージにより産生される炎症性サイトカインの一種であり、抗TNF抗体は関節リウマチや炎症性腸疾患に対して効果を発揮する。
特記事項
本研究成果は、2019年11月19日午前1時(日本時間)に英国科学誌「Nature Immunology」(オンライン)に掲載されました。
【タイトル】 “Identification of a novel arthritis-associated osteoclast precursor macrophage regulated by FoxM1”
【著者名】Tetsuo Hasegawa1,2, Junichi Kikuta1,3, Takao Sudo1, Yoshinobu Matsuura1, Takahiro Matsui1, Szandor Simmons1, Kosuke Ebina4, Makoto Hirao4, Daisuke Okuzaki5, Yuichi Yoshida6, Atsushi Hirao7, Vladimir V. Kalinichenko8, Kunihiro Yamaoka2, Tsutomu Takeuchi2, and Masaru Ishii1,3
【所属】
1大阪大学 大学院医学系研究科 免疫細胞生物学
2慶應義塾大学 医学部 リウマチ・膠原病内科
3大阪大学 免疫学フロンティア研究センター
4大阪大学 大学院医学系研究科 整形外科学
5大阪大学 微生物病研究所 遺伝情報実験センター
6大阪大学 大学院医学系研究科 消化器内科学
7金沢大学 ナノ生命科学研究所 がん進展制御研究所 遺伝子・染色体構築研究分野
8米国 シンシナティ小児病院 肺生物学部門 Division of Pulmonary Biology
本件に関して、11月15日に大阪大学・東京ブランチにて記者発表を行いました。
【報道について】
11月19日読売新聞夕刊8面、日本経済新聞オンラインに掲載されました。










