新治療薬を用いた表在性膀胱がんに対する医師主導治験を開始 ~表在性膀胱がんの再発を亜塩素酸ナトリウムで抑制~
2023年7月19日
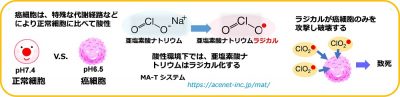 図1:亜塩素酸ナトリウムによるがん細胞の細胞死の誘導
図1:亜塩素酸ナトリウムによるがん細胞の細胞死の誘導
クリックで拡大表示します
研究成果のポイント
- 膀胱がんは男性に多く発症し、新たに診断された膀胱がんの約70%が筋層非浸潤性膀胱がん※1である。
- 筋層非浸潤性膀胱がんは内視鏡手術で切除可能であるが再発率が高く、再発抑制のためBCG※2や抗がん剤を注入する治療を行う。
- 膀胱内に注入するので刺激性が低く、継続して使用できる治療薬の開発が望まれている。
- 亜塩素酸ナトリウムは大阪大学で抗がん作用の研究が進められ、筋層非浸潤性膀胱がんの再発率を抑制し、かつ、従来の治療薬に比べて刺激性が低いことが期待されている。
- 亜塩素酸ナトリウムを用いた表在性膀胱がんに対する医師主導治験を大阪大学医学部附属病院で開始。
- 本治療薬は大阪大学大学院薬学研究科で研究され、その成果を大阪大学ベンチャーキャピタル株式会社が支援する大阪大学発ベンチャー 株式会社HOISTが引き継いで開発を実施している(HOIST社はMA-TTMシステム※3を活用した医薬品の実用化を目指している)。
概要
大阪大学大学院医学系研究科 泌尿器科学の河嶋厚成 講師らは、筋層非浸潤性膀胱がん(NMIBC)に対して行う経尿道的膀胱切除術※4(TURBT)でがん組織を切除した後、再発抑制のために亜塩素酸ナトリウム(開発コード: HM-001)を膀胱内に注入する治療法の確立を目指し、安全性と有効性を確認するための医師主導治験を、大阪大学医学部附属病院で開始しました。
本治験は第Ⅰ/Ⅱa相臨床試験であり、第Ⅰ相試験パート(パート1)ではHM-001の安全性を確認し、将来の治療で用いる薬剤用量(推奨用量)を決定します。第Ⅱa相試験パート(パート2)ではパート1で決定した推奨用量を用いた際のTURBTから1年後の膀胱がんの非再発率を確認します。
HM-001を用いた治療法が確立されれば、既に承認されて使用されている薬剤を用いた治療法で課題となっている治療継続率が改善され、また、治療継続率の改善により膀胱がんの非再発率が期待できます。本治験は、株式会社HOISTより治験薬の提供、大阪大学医学部附属病院 未来医療開発部とイーピーエス株式会社の支援を受けて実施されます。
研究の背景
これまでに、大阪大学大学院薬学研究科 細胞生理学分野の辻川和丈 教授らの研究グループは、細胞および動物を用いた試験において、亜塩素酸ナトリウムが膀胱がん細胞の増殖を抑制することを明らかにしました。
この成果を大阪大学発のベンチャー企業である株式会社HOISTが引き継ぎ、動物試験での更なる有効性の確認、GLP基準※5に基づいた安全性の確認、治験薬の製造を行っています。治験薬は、株式会社HOISTがGMP基準※6に準拠して製造し、提供しています。
本研究の内容
本治験は大阪大学大学院医学系研究科 泌尿器科学の河嶋厚成 講師が計画し、株式会社HOISTより治験薬の提供を受けて実施されます。
パート1では、NMIBC患者さんを対象にHM-001の3つの薬剤用量を設定し、低い薬剤用量から3例ずつTURBTの1週後に膀胱内へ1回注入し、4週の間隔を空けた後から週1回の膀胱内注入を6週継続します。3例毎にHM-001の安全性を第三者委員会で評価し、安全であると判断された場合には、1つ上の用量で3例の患者さんの膀胱内に注入します。治験薬に起因し、安全性に懸念が生じた場合には同じ用量で3例を追加して安全性を再度評価します。安全であると判断された場合には1つ上の用量に移ります。この手順を繰り返し、3つの薬剤用量の安全性を評価し、将来の治療で用いる薬剤用量(推奨用量)を決定します。
パート2では、NMIBC患者さんを対象に、パート1で推定された推奨用量を、パート1と同じスケジュールで導入治療を行い、その後、維持治療として週1回3週間連続での膀胱内注入を13週間隔で3回繰り返し、TURBTから57週後(約1年後)の膀胱がんの非再発率を有効性指標として評価し、また、有害事象の発現状況などの安全性の評価を行います。
登録予定の患者さんは、パート1で最大18名、パート2で30名です。
本研究が社会に与える影響
膀胱がん診療ガイドラインで推奨されているTURBT後のBCGや抗がん剤の膀胱内注入療法では、膀胱内刺激が強いことから治療継続率は高くなく、非再発率も50~80%程度にとどまっています。
TURBT後にHM-001を膀胱内に注入して膀胱内の刺激が弱いことが明らかになれば、従来の治療法に比べて治療継続率が高まり、更には膀胱がんの非再発率が高まることで、患者さんの予後およびQOL改善に繋がると期待されています。
研究者のコメント
<河嶋 厚成 講師>
筋層非浸潤性膀胱がん(NMIBC)に対する治療は膀胱温存を目指して、膀胱内視鏡を用いたがん組織の切除治療(TURBT)を行います。NMIBCの臨床的特徴は、TURBTによる治療後も高率かつ頻回に膀胱内再発を認めることであり、これは膀胱内の残存腫瘍によるものです。NMIBC治療では、TURBT後に薬剤を膀胱内に注入することで膀胱がんの再発・進展を抑制することが非常に重要とされています。
しかし、既存の薬剤では膀胱内の刺激が強く、排尿困難、頻尿や発熱等を高頻度に認めるため、ガイドライン規定の治療を継続、完遂することが難しいことが知られています。
HM-001が低刺激であってガイドラインに準じた治療の継続が可能となれば、膀胱がんの再発率を抑制することができ、患者さんのQOL、予後を改善できると考えています。
大阪大学発、世界初の治療薬開発は未だ臨床試験に着手したばかりで、実臨床で使用できる時期まで暫く時間が必要ですが、患者さんの安全性確保を第一に慎重に且つ速やかに進めてゆきたいと考えています。
用語説明
※1 筋層非浸潤性膀胱がん
(NMIBC: non-muscle invasive bladder cancer)
表在性膀胱がん(粘膜上皮内にとどまっている)及び上皮内膀胱がん(粘膜上皮内で広がっている)を指します。
 図2: 膀胱がんの深達度
図2: 膀胱がんの深達度
クリックで拡大表示します
がん情報サービスより: https://ganjoho.jp/public/cancer/bladder/treatment.html
※2 BCG
ウシ型結核菌をもとにして作製された細菌で、BCGを利用した結核に対するワクチンが知られています。BCGには膀胱がんを死滅させる効果が確認されているので、BCGは結核の予防接種だけでなく、膀胱内注入療法に応用されていますが、副作用も多く見られます。
※3 MA-TTMシステム
(Matching Transformation System)
亜塩素酸イオンから必要な時に、必要な量の水性ラジカルを発生させる酸化制御技術です。MA-TTMの価値向上と普及を目的に「日本MA-T工業会」が設立され、HOIST社も加盟しています。
※4 経尿道的膀胱切除術
(TURBT: Trans urethral resection of bladder tumor)
全身麻酔あるいは腰椎麻酔を行って、専用の内視鏡を用いてがん組織を電気メスで切除する方法で、診断をかねて実施されます。https://kompas.hosp.keio.ac.jp/contents/000255.html
 図3: 経尿道的膀胱腫瘍切除(TURBT)の術式
図3: 経尿道的膀胱腫瘍切除(TURBT)の術式
クリックで拡大表示します
※5 GLP基準
(Good Laboratory Practice)
医薬品等に対する各種安全性試験成績の信頼性を確保することを目的とした基準です。
※6 GMP基準
(Good Manufacturing Practice)
医薬品等の製造において、製造過程全体にわたって品質を確保するための基準です。










