肥後 修一朗 ≪重症心不全内科治療学≫、坂田 泰史 ≪循環器内科学≫ 筋ジストロフィー重症化メカニズムの一端を iPS細胞由来分化心筋細胞を用いて解明
- Text in English
2023年2月9日
掲載誌 JACC: Basic to Translational Science
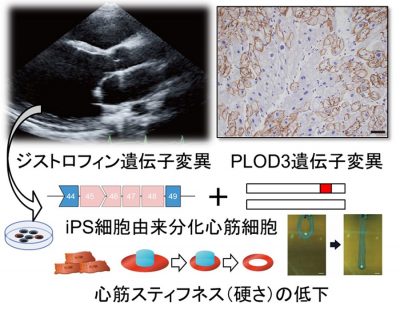 図. 重症心不全をきたしたベッカー型筋ジストロフィー女性キャリア
図. 重症心不全をきたしたベッカー型筋ジストロフィー女性キャリア
クリックで拡大表示します
研究成果のポイント
- ベッカー型筋ジストロフィーの女性キャリアが重症心不全をきたすことは極めてまれで、そのメカニズムは不明でした。
- 重症心不全をきたしたベッカー型筋ジストロフィー女性キャリア症例において、ジストロフィン遺伝子変異に加え、コラーゲン生合成に関わるPLOD3遺伝子変異を同定しました。
- 遺伝背景が同一のiPS細胞を作成し、分化させた心筋細胞を用いて、PLOD3変異が心筋スティフネス(硬さ)の低下、コラーゲン生合成の低下に関与していることを見出しました。
- ベッカー型筋ジストロフィーの重症化メカニズムを新たに発見し、今後の治療法開発につながることが期待されます。
概要
大阪大学大学院医学系研究科の肥後修一朗 特任准教授(常勤)(重症心不全内科治療学共同研究講座)、坂田泰史 教授(循環器内科学)らの研究グループは、ベッカー型筋ジストロフィーが重症心不全をきたすメカニズムを、iPS細胞由来分化心筋細胞を用いて解明しました。
今回研究グループは、補助人工心臓が必要な重症心不全に至ったベッカー型筋ジストロフィー女性キャリア症例を対象に、心筋組織病理標本を用いた解析、遺伝解析、iPS細胞から分化させた心筋細胞を用いた機能解析を行いました。解析の結果、ジストロフィン遺伝子変異に加え、コラーゲンの生合成に関わるPLOD3の遺伝子変異が存在することで、心臓組織の収縮力に加えスティフネス(硬さ)を低下させ、重症化に関与していることを見出しました。重症心不全の病態解明、今後の治療法開発につながることが期待されます。
研究の背景
現在の日本において、心臓移植が必要な重症心不全の原因の多くを拡張型心筋症※1が占めています。ベッカー型筋ジストロフィー※2は、ジストロフィン遺伝子※3の変異により発症する遺伝性の病気で、心不全の原因となる拡張型心筋症の原因となります。ジストロフィン遺伝子はX染色体※4上に存在するため、X染色体を1本しかもたない男性で発症することが多く、X染色体を2本もつ女性はキャリアとなり、男性に比べ軽症で経過することが多いとされています。ベッカー型筋ジストロフィー女性キャリアが、若くして重症心不全に至ることは極めてまれであり、その原因やメカニズムは明らかではありませんでした。
研究の内容
研究グループは、若くして補助人工心臓が必要な重症心不全に至ったベッカー型筋ジストロフィー女性キャリア症例を見出し、心筋組織病理解析、遺伝解析、iPS細胞由来分化心筋細胞を用いた機能解析を行いました。
本症例では、ジストロフィン遺伝子の45番目から48番目のエクソンが抜け落ちる遺伝子変異により、短くなったジストロフィン(Δ45-48ジストロフィン)が作られていることが分かりました。ベッカー型筋ジストロフィー女性キャリアでは、X染色体不活化※5と呼ばれるしくみにより、全身の組織で、正常なジストロフィンと短くなったジストロフィンがモザイク状に存在していますが、ヒト心臓の組織で同様の現象が起きているかは明らかではありませんでした。補助人工心臓手術時に得られた心筋組織を対象に、エクソン45を認識する抗体で免疫染色を行ったところ、正常ジストロフィンとΔ45-48ジストロフィンがおよそ6:4の比率で作られていることが明らかとなりました(図1)。
更に、本症例の重症化メカニズムを明らかにするため、詳しく遺伝子解析を行ったところ、ジストロフィン遺伝子変異に加え、PLOD3遺伝子※6にストップゲイン変異※7が生じていることが明らかとなりました。ベッカー型筋ジストロフィー女性キャリアでは、全身の細胞において、2本のX染色体がランダムにX染色体不活化を受けています。研究グループは、このX染色体不活化のしくみを利用することで、血液の細胞から作成したiPS細胞から、正常なジストロフィンまたはΔ45-48ジストロフィンを主に作り出しているiPS細胞を選別することに成功しました。更に、ゲノム編集技術を用いて、同定されたPLOD3遺伝子変異を正常に修復した、遺伝背景が同一のアイソジェニックiPS細胞※8を作成しました(図2)。これら細胞は同一の遺伝背景をもつため、病気の原因となる遺伝子の機能に焦点をあてた解析が可能となります。
作成したiPS細胞を心筋細胞に分化させ、更にリング状に組織化し、上下に伸ばす刺激を加えることで、心筋組織が収縮する力やスティフネス(硬さ)※9を測定しました。Δ45-48ジストロフィンを作り出す心筋細胞では、正常ジストロフィンを作り出す心筋細胞に比べて収縮力、スティフネスが低下し、PLOD3変異を修復することで、スティフネスが改善することが明らかとなりました(図3)。更に、組織の維持に必要なコラーゲンの産生量がPLOD3の欠損により低下し、ゲノム編集で変異を修復することで改善することが明らかとなりました。
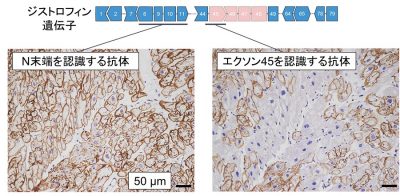 図1. 心筋組織におけるジストロフィンタンパク質発現
図1. 心筋組織におけるジストロフィンタンパク質発現
連続した2つの心臓組織切片を用いた免疫染色像です。ジストロフィンのN末端を検出する抗体はすべての
ジストロフィンタンパク質を認識しますが、エクソン45を認識する抗体はΔ45-48ジストロフィンを
認識できないため、心臓組織において両者がモザイク状に作られている様子が観察されました。
クリックで拡大表示します
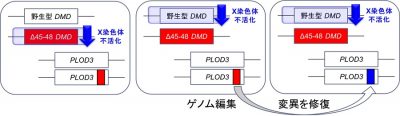 図2.X染色体不活化機構・ゲノム編集を用いたアイソジェニックiPS細胞の構築
図2.X染色体不活化機構・ゲノム編集を用いたアイソジェニックiPS細胞の構築
ジストロフィン遺伝子(DMD)は2本のX染色体上にあるため、X染色体不活化のしくみにより、どちらかが働かなくなります。このしくみを利用して、正常(野生型)またはΔ45-48ジストロフィン(DMD)がそれぞれ作られるiPS細胞を作成しました。
さらに、ゲノム編集を用いて、PLOD3遺伝子変異を正常に修復したiPS細胞を作成しました。
クリックで拡大表示します
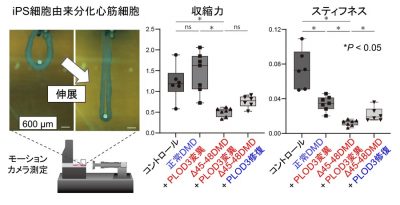 図3. 三次元組織化リングを用いた心筋収縮力・スティフネスの評価
図3. 三次元組織化リングを用いた心筋収縮力・スティフネスの評価
iPS細胞由来分化心筋細胞からリング状の組織を作成し、伸展させながらモーションカメラで測定することで、
心筋組織の収縮力、スティフネス(硬さ)を測定しました。
クリックで拡大表示します
本研究が社会に与える影響(本研究成果の意義)
原因が分からない重症心不全を克服するには、ひとつひとつの症例において、そのメカニズムを解明していくことが必要です。本症例では、ベッカー型筋ジストロフィーの原因となるジストロフィン遺伝子に加え、2つめのPLOD3遺伝子変異が存在することで、特に心筋のスティフネス(硬さ)に影響し、重症化に関わっていることが示唆されました。これら重症症例に対する今後の治療法開発につながると考えられます。
研究者のコメント
<肥後 修一朗 特任准教授 >
心臓移植が必要となる重症心不全の原因の多くは、難病である拡張型心筋症です。拡張型心筋症は、心臓が大きくなり、血液を送り出す力が低下する病気で、一見同じように見えますが、遺伝子解析技術の進歩により、幅広い原因が存在していることがわかってきました。拡張型心筋症の克服のためには、ひとりひとりの患者さんの病態に向き合い、基礎研究を行って、ひとつひとつその原因を追究していくことが重要と考えられます。
用語説明
※1 拡張型心筋症
心室が大きく広がり、心臓の筋肉が収縮する力が低下する病気で、難病に指定されています。
※2 ベッカー型筋ジストロフィー
ジストロフィン遺伝子の変異のため、ジストロフィンタンパク質が欠損するデュシャンヌ型筋ジストロフィーと、一部のタンパク質が抜け落ちて短いジストロフィンタンパク質が産生されるベッカー型筋ジストロフィーに分類されます。ベッカー型筋ジストロフィーの症例は、デュシャンヌ型筋ジストロフィーに比べ、一般に軽症で経過するとされています。
※3 ジストロフィン遺伝子
細胞の骨格を形成する遺伝子のひとつで、遺伝子変異が生じた場合、筋力の低下や心不全を生じる筋ジストロフィーを引き起こします。
※4 X染色体
性染色体のひとつで、男性では1本、女性では2本のX染色体をもちます。X染色体上に存在する遺伝子変異により発症する病気では、男性は発症者、女性はキャリアとなり、女性キャリアは、男性に比べて軽症で経過することが多いとされています。
※5 染色体不活化
女性は2本のX染色体をもつため、片方の染色体の遺伝子は働かないように抑えられており、X染色体不活化と呼ばれます。
※6 PLOD3遺伝子
組織の維持に必要なコラーゲンの作成に関わる遺伝子で、遺伝子変異により、皮膚の病気である表皮水疱症を起こすことが知られています。
※7 ストップゲイン変異
遺伝子変異のために、アミノ酸へ変換されるはずの遺伝子配列がストップコドンに変化し、タンパク質への翻訳がストップしてしまうことにより、正常なタンパク質が産生されなくなる変異です。
※8 アイソジェニックiPS細胞
ゲノム編集などを用いて作成される、対象となる遺伝子以外の遺伝的背景が同一のiPS細胞で、対象遺伝子の解析を行うのに適しています。
※9 スティフネス(硬さ)
組織の硬さを表す指標で、数値が低ければ柔らかく、数値が高ければ硬い状態を示します。
特記事項
本研究成果は、2023年2月9日(木)(日本時間)に米国科学誌「JACC: Basic to Translational Science」(オンライン)に掲載されました。
【タイトル】
“Modeling Reduced Contractility and Stiffness Using iPSC-Derived Cardiomyocytes Generated from Female Becker Muscular Dystrophy Carrier”
【著者名】
Satoshi Kameda1, Shuichiro Higo1,2,*, Mikio Shiba3, Takumi Kondo1, Junjun Li4,5, Li Liu4,5, Tomoka Tabata1, Hiroyuki Inoue1, Shota Okuno1, Shou Ogawa1, Yuki Kuramoto1, Hideki Yasutake1,6, Jong-Kook Lee1,6, Seiji Takashima7, Yoshihiko Ikeda8, Shungo Hikoso1, Shigeru Miyagawa4, Yasushi Sakata1(*責任著者)
- 大阪大学大学院医学系研究科 循環器内科学
- 大阪大学大学院医学系研究科 重症心不全内科治療学共同研究講座
- 大阪警察病院 循環器内科
- 大阪大学大学院医学系研究科 心臓血管外科学
- 大阪大学大学院医学系研究科 最先端再生医療学共同研究講座
- 大阪大学大学院医学系研究科 心血管再生医学共同研究講座
- 大阪大学大学院生命機能研究科 医化学
- 国立循環器病研究センター 病理部
【DOI番号】10.1016/j.jacbts.2022.11.007
本研究は、日本学術振興会基盤研究C(19K08489、19K12801)、基盤研究B(21H02915)、挑戦的研究(萌芽)(20K21602、22K19526)、日本医療研究開発機構再生医療実現拠点ネットワークプログラム(21bm0804008h0005、22bm0804035h0001)の支援を受けて行われました。










