内藤 龍彦、岡田 随象 ≪遺伝統計学≫ 原発性アルドステロン症の発症に関わる遺伝子を同定
~高血圧の遺伝的素因への大きな寄与を明らかに~
2023年2月21日
掲載誌 Circulation
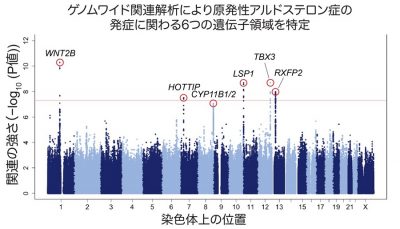 図1. 原発性アルドステロン症に関するゲノムワイド関連解析
図1. 原発性アルドステロン症に関するゲノムワイド関連解析
クリックで拡大表示します
研究成果のポイント
- 難治性高血圧の主要な原因疾患である原発性アルドステロン症※1のゲノムワイド関連解析※2を実施し、その発症に関わる複数の遺伝子領域を同定した。
- 原発性アルドステロン症は、高血圧の原因疾患の一つで、高血圧全体の約10%を占めるとされる。難治性であることが多く、脳卒中、心血管疾患、慢性腎臓病などを高頻度に合併する。まだ不明な点が多く、遺伝的因子については十分に解明されていなかった。
- 原発性アルドステロン症が高血圧の遺伝的素因の多くを占めうることを明らかにした。
- 原発性アルドステロン症の病態機序の解明に貢献し、将来的には新しい治療法や診断法の開発に繋がると期待される。
概要
大阪大学大学院医学系研究科の内藤龍彦 助教(研究当時/現:マウントサイナイ医科大学博士研究員)、岡田随象 教授(遺伝統計学/理化学研究所生命医科学研究センター システム遺伝学チーム チームリーダー/東京大学大学院医学系研究科 遺伝情報学 教授)、広島大学大学院医系科学研究科の沖健司 講師(分子内科学)、京都大学大学院医学系研究科の井上浩輔 助教(社会疫学)らの研究グループは、難治性高血圧の主要な原因疾患である原発性アルドステロン症に関するゲノムワイド関連解析を実施し、その発症に関わる複数の遺伝子領域を明らかにしました。
原発性アルドステロン症は、高血圧の原因疾患の一つであり、高血圧全体の約10%を占めると言われています。原発性アルドステロン症による高血圧は難治性であることが多く、脳卒中、心血管疾患、慢性腎臓病などを高頻度に合併します。その病態機序は不明な点が多く、特に発症に関わる遺伝的因子については十分に解明されていませんでした。
今回、研究グループは、広島大学が収集した臨床検体とバイオバンク・ジャパン※3が保有する対照検体を用いてゲノムワイド関連解析を実施し、さらにUKバイオバンク※4(英国)とFinnGen※5(フィンランド)のゲノムワイド関連解析と統合してメタ解析※6を行うことにより、原発性アルドステロン症の発症に関わる6つの遺伝子領域を同定しました(図1)。さらに、高血圧に関わる既知の遺伝子領域について、原発性アルドステロン症と高血圧におけるオッズ比※7を比較解析することで、高血圧に関わる遺伝子領域の多くが原発性アルドステロン症由来である可能性があることを示しました。
本研究成果原発性アルドステロン症の病態機序の解明に大きく貢献すると共に、将来的には新しい治療法や診断法の開発に繋がると期待されます。
研究の背景
アルドステロンは副腎※8から分泌されるホルモンであり、血圧の調整に関与しています。原発性アルドステロン症は、そのアルドステロンが過剰に分泌されることにより高血圧を来す疾患です。原発性アルドステロン症による高血圧は特に治療抵抗性の難治性高血圧を来すことが多く、脳卒中、心血管疾患、慢性腎臓病などを高率に合併します。高血圧の有病率は、本邦において成人の約2〜3分の1を占めていますが、原発性アルドステロン症はそのうち約10%の原因を占めると報告されています。さらに、正確な診断の難しさから未診断の患者さんが多く隠れている可能性も指摘されています。従って、原発性アルドステロン症の病態機序を解明し新規の治療法や診断法の開発に繋げることは公衆衛生上の観点からも重要な課題でした。これまで、原発性アルドステロン症の発症に関わる遺伝的因子については十分に解明されていませんでした。
本研究の成果
研究グループは、広島大学が収集した臨床検体とバイオバンク・ジャパンが保有する対照検体を用いてゲノムワイド関連解析を実施し、さらに国外のバイオバンクであるUKバイオバンク(英国)とFinnGen(フィンランド)のゲノムワイド関連解析の結果と統合して、原発性アルドステロン症患者群816人と対照群425,239人を対象としたメタ解析を行いました。結果、原発性アルドステロン症の発症に関わる6つの遺伝子領域(WNT2B、HOTTIP、CYP11B1/2、LSP1、TBX3、RXFP2)の遺伝子多型※9を同定しました(図1)。
原発性アルドステロン症の発症リスクと最も強い関連を認めた遺伝子多型があるWNT2Bは、細胞の増殖や分化を制御することで腫瘍の増生に関わるWnt/β–カテニン経路※10を構成するWntタンパクファミリーの一種をコードします。原発性アルドステロン症の発症においてWnt/β–カテニン経路の役割は以前から指摘されており、本研究の結果はその重要性をより強固にするものと考えられます。さらに研究グループは、副腎組織におけるeQTL (expression quantitative trait loci)解析※11とゲノムワイド関連解析の結果に対して共局在解析※12を適用することで、今回検出された遺伝子領域の1つであるRXFP2の遺伝子多型が副腎組織においてRXFP2遺伝子の発現量を上昇させることで原発性アルドステロン症の発症に関わる可能性があることを示しました。
上記の6つの遺伝子領域は、いずれも高血圧のリスクに関わる遺伝子領域として以前から報告されていましたが、本研究の結果により、それらは高血圧の中でも特に原発性アルドステロン症の発症に特異的に関わるものであることが明らかになりました。さらに、研究グループは、高血圧のリスクに関わると報告されている既知の遺伝子領域の中に、原発性アルドステロン症のリスクに起因するものが他にも隠れているのではないかと仮説を立てました。これを検証するために、高血圧のリスクに関わる既知の遺伝子領域42個の遺伝子多型について、原発性アルドステロン症におけるオッズ比と高血圧におけるオッズ比を比較解析しました。結果、42個のうち66.7%(28個)が、高血圧よりも原発性アルドステロン症に対してより高いオッズ比を示すことがわかりました(図2)。
それらは、原発性アルドステロン症の発症に関わる遺伝子領域の候補と考えられ、今後より多くの集団を対象としたゲノムワイド関連解析を実施することで、それらと原発性アルドステロン症の発症との関連をより頑健に示しうることが期待されます。また、原発性アルドステロン症が高血圧全体の約10%を占めるのに対して、高血圧の遺伝的素因に占める割合が予想外に大きい可能性があることも明らかになりました。
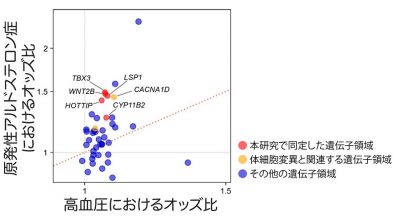 図2. 高血圧に関わる既知の遺伝子領域の原発性アルドステロン症と高血圧におけるオッズ比の比較
図2. 高血圧に関わる既知の遺伝子領域の原発性アルドステロン症と高血圧におけるオッズ比の比較
高血圧に関わる既知の遺伝子領域の半数以上が原発性アルドステロン症に関して、より高いオッズ比を示した
RNF213など一部の遺伝子領域は高血圧に関して、よりオッズ比を示した
クリックで拡大表示します
本研究が社会に与える影響(本研究成果の意義)
上述のように、原発性アルドステロン症は、その重篤性や公衆衛生上の観点から重要性の高い疾患です。本研究によって原発性アルドステロンの発症に関わる複数の遺伝子領域が明らかになったことにより、原発性アルドステロン症の病態の理解が大きく進むことが期待されます。また、将来的には創薬や診断バイオマーカーの開発に繋がることも期待されます。
研究者のコメント
<内藤 龍彦 助教(研究当時)>
ゲノムワイド関連解析研究を実施するためには、十分な検出力を得るための症例数が必須です。本研究は、正確な診断が難しいとされる原発性アルドステロン症の貴重な臨床検体を共同研究機関である広島大学大学院医系科学研究科分子内科学よりご共有していただくことで実現できました。また、対照検体はバイオバンク・ジャパンが保有するものを使用させていただきました。本研究成果が原発性アルドステロン症の病態の理解を大きく進め、新しい治療法や診断法の開発に貢献し、患者さんの診療に役立つ日が来ることを期待しております。すべての共同研究者や研究支援機構、検体をご提供していただいた方々に深く感謝を申し上げます。
用語説明
※1 原発性アルドステロン症
副腎から分泌されるアルドステロンというホルモンが過剰に分泌されることにより、高血圧や血液中のカリウム濃度の低下を引き起こす疾患。
※2 ゲノムワイド関連解析
Genome-wide association study: GWAS
ヒトゲノム配列上に存在する数百万〜数千万か所の遺伝子多型と疾患の発症の関係を網羅的に検定することで、疾患の発症に関わる遺伝子多型を特定する遺伝統計解析手法。これまで1,000を超えるヒト疾患に関わる遺伝子多型が同定されている。
※3 バイオバンク・ジャパン
日本人集団約27万人を対象とした生体試料バイオバンクで、東京大学医科学研究所内に設置されている。ゲノムDNAや血清サンプルを臨床情報と共に収集し、研究者へのデータの公開や分譲を行っている。
※4 UKバイオバンク
英国の約50万人を対象とした国家的な生体試料バイオバンク。ゲノム情報や多彩な臨床情報、追跡情報を収集し、世界中の研究者にデータの公開や分譲を行っている。
※5 FinnGen
フィンランドの国家的な生体試料バイオバンクで、稼働中のプロジェクトとして50万人規模の登録者を目指しており、研究当時は約18万人を対象としたGWASの結果サマリが公開されていた。
※6 メタ解析
統計検定における検出力の増加や各研究における偏りの調整を目的に、複数の研究結果を統合する解析手法。
※7 オッズ比
ある疾患へのかかりやすさを二つの群で比較して示したもの。オッズ比が1より大きい場合は疾患にかかりやすく、1より低い場合は疾患にかかりにくいことを示す。
※8 副腎
左右の腎臓の上部に位置し、ホルモンを産生・分泌する器官。副腎が分泌するホルモンの一つであるアルドステロンは血圧の調整に関わる。
※9 遺伝子多型
遺伝子を構成している塩基配列の個体差であり、集団中の頻度が1%以上の割合で認められるもの。
※10 Wnt/β–カテニン経路
Wntタンパクを介した細胞内シグナル伝達経路の一つであり、細胞の増殖や分化を制御する働きがある。
※11 eQTL (expression quantitative trait loci)解析
遺伝子の発現量と遺伝子多型との関連を網羅的に検定することで、ある遺伝子多型の有無である遺伝子の発現量が上昇もしくは低下するかを明らかにすること。
※12 共局在解析
GWASによる結果とeQTL解析などの結果の類似性を比較することで、それぞれの関連シグナルが同じ局在に由来するかを調べること。
特記事項
本研究成果は、2023年2月21日(火)19時(日本時間)に米国科学誌「Circulation」(オンライン)に掲載されました。
【タイトル】
“Genetic risk of primary aldosteronism and its contribution to hypertension: a cross-ancestry meta-analysis of genome-wide association study”
【著者名】
Tatsuhiko Naito1,2,3, Kosuke Inoue4, Kyuto Sonehara1,3,5, Ryuta Baba6, Takaya Kodama6, Yu Otagaki6, Akira Okada, MD6, Kiyotaka Itcho6, Kazuhiro Kobuke7, Shinji Kishimoto8, Kenichi Yamamoto1, BioBank Japan, Takayuki Morisaki9,10, Yukihito Higashi8, Nobuyuki Hinata11, Koji Arihiro12, Noboru Hattori6, Yukinori Okada1,3,5,13-15*, Kenji Oki6*(*責任著者)
- 大阪大学大学院医学系研究科 遺伝統計学
- 東京大学大学院医学系研究科 神経内科学
- 理化学研究所 生命医科学研究センター システム遺伝学チーム
- 京都大学大学院医学系研究科 社会疫学
- 東京大学大学院医学系研究科 遺伝情報学
- 広島大学大学院医系科学研究科 分子内科学
- 広島大学大学院医系科学研究科 糖尿病・生活習慣病予防医学
- 広島大学原爆放射線医科学研究所 放射線災害医療研究部門 再生医療開発研究分野
- 東京大学医科学研究所 人癌病因遺伝子分野
- 東京大学医科学研究所 内科学
- 広島大学大学院医系科学研究科 腎泌尿器科学
- 広島大学病院 病理診断科
- 大阪大学 免疫学フロンティア研究センター(IFRec) 免疫統計学
- 大阪大学 先導的学際研究機構(OTRI) 生命医科学融合フロンティア研究部門
- 大阪大学 感染症総合教育研究拠点(CiDER)
【DOI番号】10.1161/CIRCULATIONAHA.122.062349
なお、本研究は、日本医療研究開発機構(AMED)ゲノム医療実現推進プラットフォーム事業「遺伝統計学に基づく日本人集団のゲノム個別化医療の実装」の一環として行われ、大阪大学先導的学際研究機構、大阪大学大学院医学系研究科バイオインフォマティクスイニシアティブの協力を得て行われました。
本件に関して、オンラインにて記者発表を行いました。












