大阪大学で認知症のプレシジョン医療開発が始動!バイテックグローバルエレクトロニクス社と寄附講座設置のお知らせ
9月6日発表
概要
国立大学法人大阪大学(以下、大阪大学)は、次世代の認知症診断および治療の基盤を作るため、バイテックグローバルエレクトロニクス株式会社(以下、バイテック社)※1と7月1日付けで大学院医学系研究科に「認知症プレシジョン医療開発学寄附講座」(森原剛史 寄附講座教授)を設置いたしました。
認知症診断のための血液バイオマーカー※2はいまだにありません。血液バイオマーカーが実現すれば、非専門医による正確な診断や診療を可能にします。血液バイオマーカーは診断に役立つだけでなく、治療法開発にも繋がります。現在、認知症の治療薬開発が難航している大きな理由の一つは、使いやすいバイオマーカーがないからです。血液バイオマーカー開発のためには、臨床医学、基礎医学と計測工学の融合が重要です。このような考えに、半導体や電子機器の計測装置を扱っているバイテック社の理解と支援を得ました。
寄附講座ではバイオマーカー開発や、バイオマーカーと連携した認知症病態解明を進めることによって、生物学的特徴に従った新たな認知症の分類を行います。病気を生物学的に均一に細分類することにより、治療法の効率的な開発が可能になります(プレシジョン医療※3)。このように認知症のプレシジョン医療の開発に特化した講座が大阪大学に新たに開設されました。
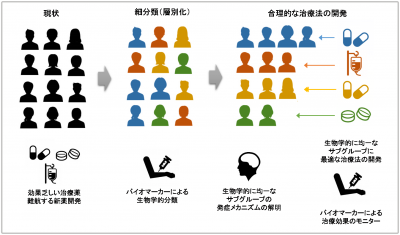
正確な診断のためにアルツハイマー病をはじめとする認知症の克服はなぜ難しいか
患者数が多く、その克服が強く求められているアルツハイマー病ですが、その効果的な治療法の開発は難航しています。なぜアルツハイマー病の克服は難しいのでしょうか?その原因として「疾患が複雑」「疾患が不均一」「使いやすいバイオマーカーがない」がよく挙げられています。寄附講座では病態解明とバイオマーカー開発を統合的に行いこれらの問題を解決します。
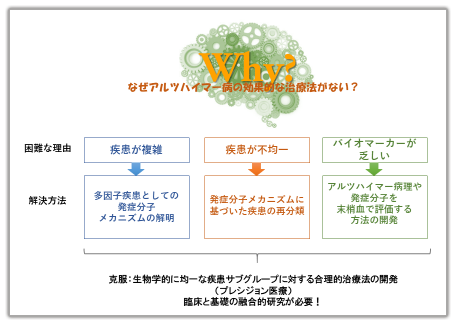
正確な診断のために
ヒトの認知機能は複雑であり、正確かつ包括的な評価は容易ではありません。認知症専門医や心理士は記憶、言語、視空間認知などを神経心理学的に診察し評価します。本人と家族・介護者に問診を行い、精神症状や神経症状、日常生活活動(ADL)を評価し、日常生活で何が問題になっているかを明らかにします。本人の教育歴や生活歴等も詳しく聞き取り、病前機能の推定や、認知症の危険因子なども把握します。認知機能に影響を与える身体疾患の鑑別や身体的基礎疾患の把握のため血液検査なども行います。必要に応じて脳画像検査も行い、脳萎縮や脳機能の低下を把握します。これらは時間も労力もかかり、患者・介護者の協力も必要です。経験のある専門医も必要になりますが、その数は限られています。
また、臨床診断の問題は上述のような多大な労力だけではありません。その精度も問題です。アルツハイマー病をはじめとする認知症の多くの確定診断は病理診断ですが、臨床診断と病理診断※4が一致しないことは珍しくありません。
認知症の臨床診断が複雑であったり、その診断精度に限界があったりするのはなぜでしょうか?使いやすいバイオマーカーがないことが大きな理由です。糖尿病の血糖値やHbA1c(ヘモグロビンエーワンシー)、脂質異常症のLDLコレステロール値のような血液バイオマーカーが認知症にはありません。専門医の診断をより正確にし、非専門医の診療もサポートし、また生活情報等を知らせてくれる家族・介護者がいない患者さんに対しても適切な診断をすることができる、安価で使いやすいバイオマーカーが求められています。
革新的な治療法開発のために
現在、臨床現場で使われているアルツハイマー病の治療薬の効果は極めて限定的です。治療薬そのものがない認知症もたくさんあります。認知症の新薬開発は精力的に行われていますが失敗が続いています。失敗の要因の一つとして、血液バイオマーカーがないことがしばしば挙げられています。臨床治験にふさわしい患者群の合理的抽出や、治療効果判定に使える血液バイオマーカーがまだありません。例えるなら、血糖値が測定できないのに糖尿病の薬を、コレステロール値が測定できないのに脂質異常症の新薬を開発している状態といえるかもしれません。もっと例えるなら、糖尿病の薬の効果を、血糖値が使えず、脳卒中など糖尿病悪化によって引き起こされる症状のみに頼って評価しているといえるかもしれません。認知症の血液バイオマーカー実用化は、革新的な治療法の開発も強力に後押しします。
その先にあるプレシジョン医療のために
例えば、脳卒中は、糖尿病や高脂血症など様々な基礎疾患が悪化し血管への負担が増えていることによりひき起こされます。脳卒中の抑制は、各患者さんがどのような基礎疾患を持っているか明らかにし、患者さんごとに異なる治療、つまりある方は糖尿病、別の方は高脂血症や高血圧の治療を行うことで実現しています。患者さんの数は、脳卒中以上にアルツハイマー病でさらに多いことが知られています。アルツハイマー病のアミロイドPETを用いた脳病理研究によると、90歳では実に70%の方でアミロイドβが脳に蓄積されていると推計されています。しかし、大勢のアルツハイマー病患者さんが全員同一の仕組みで発症するのではなく、発症の原因や脳の状態には多様性があると考えられています。アルツハイマー病の状態や発症要因の多様性を分子レベルで解明し、対応する血液バイオマーカーを開発すればアルツハイマー病をいくつかのサブグループに分類しなおすことができます。このサブグループは発症メカニズムも含め生物学的に均一になるため、それに応じた合理的な治療法の開発が効率的に行えます。
このような疾患の生物学的な再分類と、この再分類に基づく効率的な治療はプレシジョン医療とよばれ、がん治療分野では成功を収めつつあります。プレシジョン医療による治療の合理化は医療費を節約することも期待されています。
臨床医学、基礎医学と計測工学の融合
血液バイオマーカーの開発やプレシジョン医療の実現のためには、充実した認知症臨床研究、革新的な計測方法と、この両者を結ぶ基礎医学が必要です。大阪大学 大学院医学系研究科 精神医学(池田学教授)では、認知症の臨床だけでなくその基礎的な研究も精力的に行ってきました。認知症の臨床治験の実施やそのために必要な人材を育成するための寄付講座(行動神経学・神経精神医学寄附講座)も昨年開講しています。
森原寄附講座教授らは、これまでにアルツハイマー病になりやすい体質を持つマウスからその原因遺伝子Klc1を同定しています。この遺伝子産物であるKLC1vE※5タンパク質を用いて血液バイオマーカーの開発を検討しています。また、台湾のベンチャー企業(MagQu社)の革新的技術であるImmunomagnetic reduction(IMR)※6を導入し、その改良により開発を進めていきます。さらに、大阪大学の良質な診療に裏付けられた臨床検体を用いることで、バイオマーカー開発が加速されることが期待できます。また、認知症に関する他のバイオマーカーについても研究し、これらのバイオマーカーが捉えている病態を特定し、治療法の開発につなげることにより、従来とは異なる認知症の診断と治療の実現を目指しています。
用語説明
※1 バイテックグローバルエレクトロニクス株式会社
東京都品川区北品川2丁目32番3号
代表取締役社長:今野邦廣 寄付に関する担当者:戸毛栄治
業務内容:各種半導体・デバイス、計測機器の販売 ソリューション提案、技術開発サポート、ODM等のビジネス コーディネート
※2 認知症診断のための血液バイオマーカー
現在、認知症バイオマーカーとして、画像バイオマーカーと体液バイオマーカーがある。画像バイオマーカーは脳の形態を調べるMRIなどや、機能を調べる脳血流SPECT(Single Photon Emission Computed Tomography)、FDG (フルオロデオキシグルコース)-PETがあり、診断の補助に役立っている。他にアミロイドPETがあり、アルツハイマー病の診断により有用であるが、大がかりな装置が必要で、検査費用も極めて高価である。体液バイオマーカーとしては、脳脊髄液中のアミロイドβやタウの定量がアルツハイマー病診断に有用であるが、脳脊髄液の採取は通常の採血よりも侵襲的で、腰椎穿刺に慣れた医師も必要となる。
認知症には、血液バイオマーカーはまだ開発されていない。侵襲性が低く(被検者の負担が少ない)、費用も低く、繰り返しの検査やスクリーニング検査にも使用できる認知症血液バイオマーカーの開発が望まれている。
※3 プレシジョン医療
一つの疾患に対し、一つの治療法を試すというのではなく、従来の疾患をバイオマーカーで細分類(層別化)し、サブグループごとに最適化した治療を試みるという医療。がん領域では大きな成果を上げており、2015年にはオバマ大統領(アメリカ合衆国)の一般教書演説でも取り上げられ注目されている。似た概念として、パーソナライズド・メディシンがあるが、これは個人レベルでの医療の最適化を目指すもので、富裕層向けになりがちである。プレシジョン医療は疾患の層別化であり、無効な治療の抑制や治療の効率化をもたらす。また、新規治療法の開発においても、無駄を省き効率化することで、医療や治療法開発の費用の抑制も期待されている。
※4 臨床診断と病理診断
専門医が行う臨床診断は、確定診断にはならない。アルツハイマー病の確定診断は、剖検脳などを用いた病理診断まで行う必要がある。亡くなられた後、病理医が開頭して脳を取り出し、各認知症疾患の特徴となるタンパク質の蓄積状態を評価するなどして確定診断を行う。専門医や専門機関でも臨床診断と病理診断の不一致例は珍しくなく、臨床診断の感度は77.7%、特異性は85.4%などという報告がある(J Alzheimers Dis 2014 v42 p169など)。
※5 アミロイド病理規定遺伝子産物KLC1vE(kinesin light chain-1 splice variant E)
大阪大学では、アルツハイマー病の中心病理であるアミロイドβタンパク質の脳内蓄積量を規定する遺伝子産物KLC1vEを発見した(Morihara et.al. PNAS 2014など)。アルツハイマー病患者およびアルツハイマー病モデルマウスにおいては、KLC1vE メッセンジャーRNA量が脳と末梢血で高値であったことから、血液バイオマーカーとして開発を進めている。
また、KLC1vEを基盤とする孤発性アルツハイマー病の発症メカニズムの研究も進んでいる。これらの発見は、複雑な孤発性アルツハイマー病の一面が分子レベルで解明されるだけでなく、不均一な孤発性アルツハイマー病の層別化にもつながる。層別化とは、アルツハイマー病のような不均一な疾患群から、均一な生物学的性質を共有する患者群を抽出することで、層別化された患者群に対しては、治療法の開発が効率的に進めやすくなる。
※6 Immunomagnetic reduction (IMR) ;免疫性磁性低減
従来とは全く異なる原理によるターゲットタンパク質の測定方法。測定ターゲット分子に対する抗体を結合させた極小サイズ(直径50~60nm)のナノ磁性体と血液などの検体を混ぜ合わせる。ナノ磁性体に磁界をかけ回転させ、その回転で生じる磁器信号を超伝導量子干渉素子で検出する。ナノ磁性体が測定ターゲット分子と結合しているとこの回転は低下し、信号も弱まることを利用してターゲット分子量を定量する(Immunomagnetic reduction (IMR))。従来のELISA法などと比べて、IMRは100倍から1000倍の高感度であり、これまで困難であった血液中の微量タンパク質の定量が可能となった。IMRは、物理学者である楊謝樂博士が創業した台湾ベンチャー企業MagQu社により考案・作成された。このIMR測定装置を、2018年9月に大阪大学の認知症プレシジョン医療開発学寄附講座に設置する予定である。










