清水 幹人、白石 直之、多田 智、奥野 龍禎、望月 秀樹 ≪神経内科学≫、山下 俊英 ≪分子神経科学≫ 筋萎縮性側索硬化症(ALS)におけるRGMaの役割を解明
~異常タンパク凝集抑制による新規治療に期待~
2023年11月23日
掲載誌 Science Advances
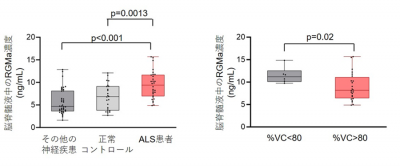 図1: RGMaはALSのCSF中で増大する(左)、CSF中のRGMa濃度が高いほど、肺活量(%VC)が低い(右)クリックで拡大表示します
図1: RGMaはALSのCSF中で増大する(左)、CSF中のRGMa濃度が高いほど、肺活量(%VC)が低い(右)クリックで拡大表示します
研究成果のポイント
- 筋萎縮性側索硬化症※1(ALS)は運動ニューロンの変性により、筋萎縮が進行する原因不明で致死的な疾患である。本研究ではALS患者の脳脊髄液(CSF)において、軸索ガイダンス因子であるRepulsive guidance molecule-a(RGMa) ※2が増加していることを発見した。また脳脊髄液中のRGMa濃度が高いとALS患者の症状が悪化する傾向があった。
- 培養神経細胞での検討ではRGMaは神経細胞のバリア機能を低下させ異常タンパクの細胞内への侵入(プロパゲーション※3)を促進させていた。またALSモデルマウスに対する抗RGMa抗体の投与により異常タンパクの凝集が軽減し生存期間が有意に延長した。
- RGMaはALSにおける予後予測バイオマーカーとなるだけではなく、中和抗体が新規治療の候補となる可能性がある。
概要
大阪大学 大学院医学系研究科の奥野龍禎 准教授、清水幹人 招へい教員、多田智 招へい教員、望月秀樹 教授(神経内科学)、山下俊英 教授(分子神経科学)らの研究グループは、筋萎縮性側索硬化症(ALS)に、RGMaが関与していることを解明しました。
RGMaは神経系の発達において細胞骨格制御により成長円錐の崩壊を誘導する軸索ガイダンス因子として同定された分子ですが、神経細胞死や軸索障害にも関与するため脊髄損傷や多発性硬化症など様々な神経疾患において治療ターゲットとして注目されていました。しかしながらALSにおける役割はこれまで検討されていませんでした。
今回の研究でALS患者の脳脊髄液でRGMaが増加していることを発見しました(図1)。また培養細胞における検討では、RGMaは、細胞骨格動態を変化させることで神経細胞のバリア機能を低下させ異常タンパクの細胞間伝播(プロパゲーション)を促進することを明らかにしました。ALSモデルマウスにおいても、抗RGMa抗体投与により異常タンパクの凝集が軽減し生存期間が有意に延長することから、RGMaはALSにおいて蛋白凝集を介して病態に重要な役割を果たしていることが明らかになりました。
本研究の背景
筋萎縮性側索硬化症(ALS)は徐々に筋力低下・筋萎縮が進行し、数年の経過で最終的には嚥下機能・呼吸機能の低下を来し死亡する、重篤な運動ニューロンの変性疾患です。その原因はまだ十分に明らかになっていませんが、異常タンパク質が脊髄前角細胞に蓄積することが一つの原因であると考えられています。またこのタンパク質の異常蓄積が細胞間を伝播し広がることで、病状が悪化することが知られており、プロパゲーションと呼称されます。このプロパゲーションはALS以外にもアルツハイマー病やパーキンソン病などのタンパク質が中枢神経に異常蓄積する疾患全般に想定されている病態であり、この制御ができれば神経変性疾患の進行を抑えられると考えられてきました。しかし現時点ではこのプロパゲーションを抑制する治療はまだ十分に考案されていません。
本研究の内容
まずALS患者の脳脊髄液中におけるRGMaが増加する事を見出しました。脳脊髄液中のRGMa濃度はALSの呼吸状態と相関がみられ、病勢を予測するバイオマーカーとして使用できることも確認しました。また抗RGMa抗体を田辺三菱製薬株式会社より提供いただき、ALS動物モデルであるG93A変異SOD1トランスジェニックマウス(mSOD1マウス)に使用したところ、寿命の延長と臨床症状の軽減が得られ(図2)、変異SOD1蛋白の凝集が低下することを発見しました(図3)。さらにこの動物モデルと培養細胞を用いた解析により、RGMaはアクチンを中心とした細胞骨格動態を変化させて神経細胞の異常蛋白に対するバリア機能を低下させ、異常蛋白のプロパゲーションを促進することでALS病態を悪化させていることが明らかとなりました。
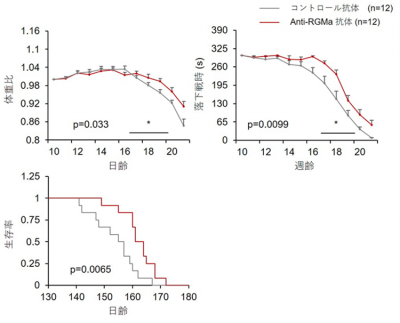 図2: 抗RGMa抗体投与によりmSOD1マウスの体重減少は軽減(上段左)
図2: 抗RGMa抗体投与によりmSOD1マウスの体重減少は軽減(上段左)
ローターロットからの落下するまでの時間(落下時間)が延長した(上段右)
また抗RGMa抗体投与により生存期間が延長した(下段)
クリックで拡大表示します
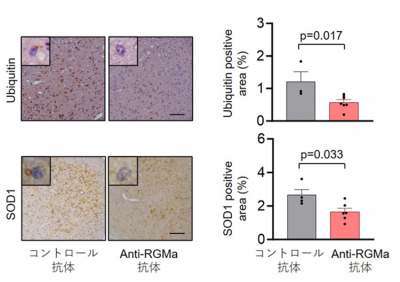 図3: 抗RGMa抗体投与によりmSOD1マウスの脊髄内でユビキチン陽性(上段)
図3: 抗RGMa抗体投与によりmSOD1マウスの脊髄内でユビキチン陽性(上段)
SOD1陽性(下段)の凝集体の沈着が低下した
左がコントロール抗体投与、右がRGMa抗体投与
クリックで拡大表示します
本研究が社会に与える影響(本研究成果の意義)
致死的疾患であるALSの中枢神経においてRGMaが増加して細胞骨格動態を変化させることによりバリア機能を低下させ異常タンパクのプロパゲーションを促進するという新しい病態機序を示すと共に、バイオマーカーや治療ターゲットとして有望であることを明らかにしました。この結果により、ALSだけでなくアルツハイマー病やパーキンソン病などプロパゲーションを介して病態が悪化する様々な疾患に対して、全く新しい治療戦略の可能性を提供できたものと考えます。
研究者のコメント
<清水幹人(招聘教員)のコメント>
ALS患者さんの脳脊髄液におけるRGMa増加とALSモデルにおけるRGMa抗体の有効性を見出した後、RGMaとALSを結びつける病態の考察と証明に難渋しましたが、試行錯誤の末ALSの新しい病態を発見することができました。ALS、RGMa、神経病理、神経細胞培養、動物実験をそれぞれ専門とする共著者の先生方から多大な援助をいただいたお陰です。この結果が新たな診断法や治療法開発の一助となれば大変嬉しく思います。
用語説明
※1 筋萎縮性側索硬化症
運動ニューロン障害により徐々に筋力低下・筋萎縮を呈し、最終的に数年で呼吸筋障害を認めて、死亡にいたる重篤な神経変性疾患。
※2 Repulsive guidance molecule-a(RGMa)
反発性軸索ガイダンス因子の一種。RhoAの活性化などを介して、細胞骨格を制御し成長円錐の崩壊を引き起こす。
※3 プロパゲーション
異常なたんぱく質の蓄積が細胞間を伝播して障害を広げてゆく病態のこと。
特記事項
本研究成果は、2023年11月23日午前4時(日本時間)に米国科学誌「Science Advances」(オンライン)に掲載されました。
【タイトル】
“RGMa collapses the neuronal actin barrier against disease-implicated protein and exacerbates ALS”
【著者名】
Mikito Shimizu1, Naoyuki Shiraishi1, Satoru Tada1,2, Tsutomu Sasaki1, Goichi Beck1, Seiichi Nagano1,3, Makoto Kinoshita1, Hisae Sumi1,4, Tomoyuki Sugimoto5, Yoko Ishida1, Toru Koda1, Teruyuki Ishikura1,4, Yasuko Sugiyama1, Keigo Kihara1, Minami Kanakura1,6, Tsuneo Nakajima7, Shuko Takeda8,9, Masanori P. Takahashi1,6, Toshihide Yamashita10*, Tatsusada Okuno1*, Hideki Mochizuki1(*責任著者)
- 大阪大学 大学院医学系研究科 神経内科学
- 大阪南医療センター
- 大阪大学 大学院医学系研究科 神経難病認知症探索治療学
- 市立東大阪医療センター 脳神経内科
- 滋賀大学 データサイエンス学部 データサイエンス学科
- 大阪大学 大学院医学系研究科 保健学専攻 臨床神経生理学研究室
- 大阪大学 大学院医学系研究科 老年・総合内科学
- 大阪大学 大学院医学系研究科 臨床遺伝子治療学
- 大阪精神医療センター
- 大阪大学 大学院医学系研究科 分子神経科学
本研究結果は、日本学術振興会・科学研究費補助金「基盤研究(C)」、日本医療研究開発機構などの支援、共同研究先の田辺三菱製薬株式会社からの資金援助を受けて行われました。また田辺三菱製薬株式会社からRGMa中和抗体の提供を受けました。










