加藤 聖也、疋田 隼人、竹原 徹郎 ≪消化器内科学≫ 肝臓のうっ血が肝臓病を引き起こす仕組みを解明
~新たな治療標的を同定~
2025年2月27日
掲載誌 Gastroenterology
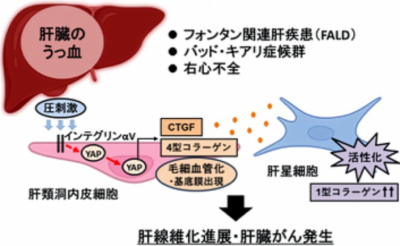
図1:肝うっ血に対する肝類洞内皮細胞の力学的応答クリックで拡大表示します
研究成果のポイント
- 慢性的な肝臓のうっ血が肝線維化や肝臓がん発症を引き起こすメカニズムを解明
- これまで肝臓のうっ血がなぜ肝線維化を引き起こすのか詳細は不明だったが、マウスモデルやヒト臨床検体に対するシングルセル解析や空間トランスクリプトーム解析を行うことで明らかに
- 肝臓のうっ血が生じる疾患に対する肝線維化を抑制する治療法の開発、さらに肝硬変治療への応用に期待
概要
大阪大学大学院医学系研究科消化器内科学大学院生の加藤聖也さん(研究当時:博士後期課程、現在:大阪大学医学部附属病院医員)、疋田隼人 准教授(配信当時:講師)らの研究グループは、小児心臓手術(フォンタン※1手術)後などに起こる肝臓のうっ血※2が肝線維化や肝臓がん発症に至るメカニズムとして、肝類洞内皮細胞※3のYAP※4の活性化やCTGF※5の発現が重要であることを世界で初めて明らかにしました。
これまで、フォンタン手術後の問題として、肝臓にうっ血が生じることにより若年で肝臓が固くなり、肝硬変や肝臓がん発症に至る症例が存在することがわかっています。肝うっ血による肝臓の線維化※6は肝臓の炎症をほとんど伴わないため、他の慢性肝障害と異なる線維化メカニズムがあると考えられていましたが、そのメカニズムについては解明されていませんでした。
今回、研究グループは、肝臓にうっ血を起こすマウスモデルの肝臓を単一細胞レベルで解析(シングルセル解析※7)することにより、肝類洞内皮細胞のインテグリンαV※8がYAPの活性化やCTGFの発現を制御しており、肝臓の線維化や肝臓がんの発生に重要であることを解明しました(図1)。さらにフォンタン手術後の肝臓に対して、空間トランスクリプトーム解析※9を行うことで、ヒトでも同様の現象が起こっている可能性が示されました。これにより、肝類洞内皮細胞のインテグリンやYAP、CTGFを阻害・抑制する治療が有効である可能性が期待されます。
本研究成果は、米国科学誌「Gastroenterology」に、2月27日(金)19時(日本時間)に公開されます。
本研究の背景
先天性心疾患の一つである単心室症に対するフォンタン手術により長期予後は劇的に改善されましたが、近年新たな問題として、肝臓にうっ血が生じることにより若年(早ければ10歳-20歳代)で肝硬変や肝臓がん発症に至る症例が存在することがわかってきました。日本では年間約400件のフォンタン手術が行われており、このようなフォンタン手術後の肝障害はFALD(Fontan-associated liver disease)と呼ばれ、罹患率は約50%とも言われています。進行することで肝硬変に至る肝臓の線維化は肝臓の慢性的な炎症を背景に起こりますが、肝臓のうっ血では肝臓の炎症はほとんど伴いません。それにも関わらず肝硬変や肝臓がんを発症するため、臨床の現場においても発症メカニズムの解明や治療法の開発が重要な課題となっていました。
本研究の内容
研究グループでは、肝うっ血を引き起こすマウスモデルを作成し、肝臓に対するシングルセル解析を行うことで、病態初期から線維化周囲(中心静脈周囲)の肝類洞内皮細胞でYAPの活性化やCTGFの著明な発現上昇が起こっていることを発見しました(図2)。
細胞実験では、肝類洞内皮細胞のインテグリンαVが、圧負荷を感知するメカニカルセンサーとしてYAP活性化やCTGF発現を制御していることがわかりました。また、肝うっ血マウスモデルに対してインテグリンαV阻害剤の投与や肝類洞内皮細胞のCTGF欠損を行うことで、肝線維化や門脈圧亢進は抑制され、後者では肝癌の発症も抑制されることもわかりました(図3)。
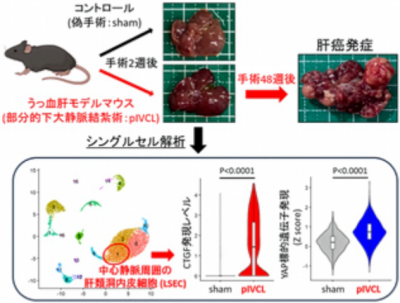 図2:うっ血肝モデルマウスの作製とシングルセル解析クリックで拡大表示します
図2:うっ血肝モデルマウスの作製とシングルセル解析クリックで拡大表示します
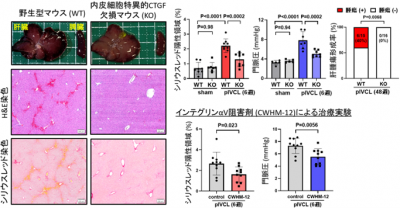 図3:内皮細胞のCTGF欠損やインテグリンαV阻害剤投与により、肝うっ血による病態進展が抑制されるクリックで拡大表示します
図3:内皮細胞のCTGF欠損やインテグリンαV阻害剤投与により、肝うっ血による病態進展が抑制されるクリックで拡大表示します
さらに、フォンタン手術後の肝臓を用いたシングルセル解析や空間トランスクリプトーム解析により、ヒトにおいても肝うっ血により肝類洞内皮細胞のYAP活性化やCTGF発現上昇が病態初期から起こり、肝星細胞の1型コラーゲン産生や肝類洞内皮細胞の4型コラーゲン産生に関与している可能性が示されました(図4)。
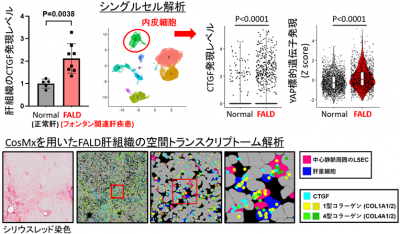 図4:フォンタン関連肝疾患(FALD)のシングルセル解析・空間トランスクリプトーム解析クリックで拡大表示します
図4:フォンタン関連肝疾患(FALD)のシングルセル解析・空間トランスクリプトーム解析クリックで拡大表示します
本研究が社会に与える影響(本研究成果の意義)
本研究成果により、フォンタン手術後などの肝臓のうっ血に対し、肝類洞内皮細胞のインテグリンαVやYAP、CTGFを阻害・抑制する治療が有効である可能性が期待されます。特にFALDにおいては若年での肝硬変・肝臓がん発症が深刻であり、有効な治療法の開発が期待されます。また、肝うっ血では、肝臓の中にあるとても細い血の通り道(肝類洞)に圧力がかかります。実は、この「通り道に圧がかかる」状態は、肝硬変でも同じように起こります。そのため、この研究は肝うっ血だけでなく、肝硬変全般の治療にも役立つ可能性があります。
研究者のコメント
<疋田 隼人 准教授(配信当時:講師)のコメント>
今回の研究により、肝臓のうっ血が続くと、血清ALT値が正常であっても肝臓が徐々に固くなり、やがて肝臓がんが発生する仕組みの一部が明らかになりました。肝うっ血で生じる「肝臓の細い血の通り道に圧がかかる状態」は、肝硬変でも同じように起こります。そのため、今回の発見は肝うっ血だけでなく、肝硬変に対する治療にも応用できる可能性があります。今後は、この知見をもとに、新しい治療法の開発につなげていきたいと考えています。
用語説明
※1 フォンタン手術
先天性心疾患の一つである単心室症に対する根治手術。上・下大静脈を肺動脈に直接つなぐことで循環を保つが、中心静脈圧が上昇するため肝臓のうっ血などの合併症が起こることが知られている。
※2 肝臓のうっ血
大静脈圧の上昇(フォンタン手術後、右心不全)や肝臓の流出路の閉塞(バッド・キアリ症候群)などにより、肝臓に血液が停滞する状態。慢性的な肝うっ血が起こると、肝臓の炎症を反映する血清ALT値が正常でも肝線維化が起こることが知られている。
※3 肝類洞内皮細胞
肝臓の類洞(門脈と中心静脈の間)に位置する内皮細胞であり、通常は存在する基底膜(細胞の足場となるシート状の薄い膜)が存在しないユニークな内皮細胞。肝疾患のゲートキーパーとして近年注目されている。
※4 YAP (Yes-associated protein)
Yes-associated protein。細胞質から核内に移行することで、転写共役因子として様々な遺伝子の転写活性をもつ。また、細胞内で機械的シグナルを伝達する役割をもつ。
※5 CTGF
connective tissue growth factor:結合組織増殖因子。血管新生や線維芽細胞の活性化、組織のリモデリング、癌の進展など、幅広い生物学的活性をもつ分泌タンパク。
※6 肝臓の線維化
慢性的な肝臓の障害に対する組織修復の結果、肝臓にコラーゲンなどの線維が沈着し肝臓が固くなる(線維化)。肝線維化が進行すると、最終的には肝硬変に至り正常な肝臓の機能が失われ様々な合併症が生じる。
※7 シングルセル解析
次世代シークエンサーにより、1細胞あたりの遺伝子発現を網羅的に解析する技術。
※8 インテグリンαV
インテグリンは細胞表面に存在する受容体であり、機械的刺激を感知し、そのシグナルを細胞内に伝達する役割をもつ。α鎖・β鎖で構成され、αVはα鎖のサブユニットである。
※9 空間トランスクリプトーム解析
組織上で1細胞単位でのトランスクリプトームの発現・分布を解析する技術。シングルセル解析では失われる組織上の位置情報が保持されることが最大のメリットとなる。
特記事項
本研究成果は、2026年2月27日(金)19時(日本時間)に米国科学誌「Gastroenterology」(オンライン)に掲載されます。
【タイトル】
“Activation of the integrin αV–YAP–CTGF axis in liver sinusoidal endothelial cells promotes liver fibrogenesis, leading to portal hypertension and liver carcinogenesis in congestive hepatopathy”
【著者名】
Seiya Kato1, Hayato Hikita1,2, Osamu Tsukamoto3,4, Katsuhiko Sato1, Kohei Kamizono1, Yoichi Sasaki1, Kenji Fukumoto1, Yuta Myojin1, Kazuhiro Murai1, Yuki Tahata1, Yuki Makino1, Yoshinobu Saito1,2, Takahiro Kodama1, Daisuke Motooka5, Shogo Kobayashi6, Hideki Yokoi7,8, Masashi Mukoyama7, Yoshiaki Kubota9, Tomohide Tatsumi1, Hidetoshi Eguchi6 and Tetsuo Takehara1* (*責任著者)
所属:
- 大阪大学大学院医学系研究科 消化器内科学
- 大阪大学先導的学際研究機構 生命医科学融合フロンティア研究部門
- 大阪大学大学院生命機能研究科 医化学
- 兵庫医科大学医学部 生化学
- 大阪大学微生物病研究所附属 バイオインフォマティクスセンター
- 大阪大学大学院医学系研究科 消化器内科学
- 熊本大学大学院生命科学研究部 腎臓内科学
- 京都大学大学院医学系研究科 腎臓内科学
- 慶應義塾大学医学部 解剖学
DOI:https://doi.org/10.1053/j.gastro.2025.11.014
なお、本研究は、日本医療研究開発機構(AMED)肝炎等克服実用化研究事業(JP24fk0210137)の一環として行われました。
【SDGs目標】
![]()
【参考URL】
疋田 隼人 准教授
研究者総覧URL:https://rd.iai.osaka-u.ac.jp/ja/b23b5f0ae68a066b.html










