木村 文隆 ≪統合生理学≫ 大脳皮質細胞のカラム状投射形成のメカニズム
~大麻の接種が脳の神経回路形成に悪影響を与えることを証明~
2022年9月6日
掲載誌 Proceedings of the National Academy of Sciences of the United States of America (PNAS)
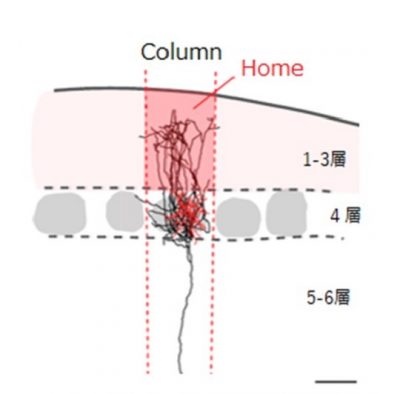 図1.大脳皮質細胞の神経線維
図1.大脳皮質細胞の神経線維
クリックで拡大表示します
研究成果のポイント
- 大脳皮質細胞のカラム状投射形成のメカニズムを初めて明らかにした
- 発達期に、神経の間違った配線がカンナビノイド*1により刈り込まれることによって、大脳皮質細胞がカラム(円柱)状に成形されることを見出した
- 内因性カンナビノイドが大脳皮質細胞のネットワーク形成に重要な役割を果たし、大麻摂取が大脳皮質細胞にダメージを与えることを直接的に証明した
- 今後、大脳皮質の情報処理の共通原理の理解が進むと期待される
概要
大阪大学大学院医学系研究科の木村文隆招へい教授(統合生理学、研究当時:分子神経科学、現:滋慶医療科学大学医療科学部教授)らの研究グループは、大脳皮質の細胞が軸索をカラム状に投射するメカニズムを明らかにしました。
大脳皮質の細胞は、その機能にかかわらず、カラム(円柱)と呼ばれる脳表面に垂直な細胞集団を構成しますが、これは情報処理の基本的単位と考えられ、高等動物の知性を担う重要な構造と想定されています(図1)。各細胞が自身の属するカラム内だけに選択的に神経線維を伸ばす、いわゆるカラム状投射を示す細胞が多くありますが、どのようなメカニズムでこのような投射が形成されるのかはほとんど解っていませんでした。今回、研究グループは、脳内伝達物質の1つである、カンナビノイドを合成することが出来ないマウスではカラム状投射が崩壊していることから(図2)、脳内カンナビノイド(内因性カンナビノイド)がカラム状投射形成に、重要な役割を果たす事を解明しました。この実験では、カンナビノイドを投与すると、大脳皮質細胞の神経線維の全長が短縮している(刈り込まれている)事を示しましたが、この結果はカンナビノイド(大麻の有効成分)を摂取すると、大脳皮質細胞の神経線維が短縮する事を示唆しています。今回の成果により、大麻を摂取すると、神経回路形成に重大な悪影響を与えることが示唆されます。
研究の背景
大脳皮質にカラム状の構造がある事は、1950年代から知られ、その後の研究によりこの構造が、高等動物の新皮質に共通の構造であり、情報処理の機能的単位となる事が明らかにされ、大脳皮質が担う高次機能の要であると考えられてきました。各カラム内では神経細胞が、その出力線維(軸索)をカラム内に選択的に伸ばしており、これをカラム状投射と呼びますが、これがカラム構造の中核をなすと考えられています。しかしながら、発達過程において、どのようなメカニズムでカラム状投射が形成されるのかということについては、ほとんど解っておりませんでした。これまでの研究では、発達期に、なんらかのメカニズムで、かなり正確に自己カラム内に選択的に神経線維を伸ばすことが知られていましたが、実験的操作や遺伝子改変動物でもカラム状投射が崩壊した例を報告したものが無く、関与する分子については明らかになっていませんでした。
研究の内容
研究グループでは、内因性カンナビノイドである、2-アラキドノイルグリセロール(2-AG)の合成酵素であるジアシルグリセロールリパーゼαを遺伝的に欠損した動物(DGLα-KO)で、大脳皮質4層細胞の軸索投射を調べたところ、カラム状投射が崩壊していました。発達を追って軸索投射形成を調べてみると、4層細胞は生後6-7日目から軸索を伸ばし始めますが、最初は深層(5~6層)方向に伸ばし、その後次第に本来の投射先である2/3層へ向けて投射が逆転します。この時、生後12日頃までは自己カラムを越えて隣接カラムにまで軸索を伸ばしている細胞も多数ありました。しかし、4層細胞の軸索末端にカンナビノイド受容体(CB1R)が発現し出す生後13日頃以降では、隣接カラムに侵入する軸索は次第に減っていき、自己カラム内へ軸索を伸ばすように、修正されていました。
一方、DGLα―KO動物では、生後12日頃までは野生型動物との差は見られませんが、13日頃以降になっても隣接カラムに侵入する軸索はそのまま残ったままでした。このことから、隣接カラムに侵入する軸索が、選択的にカンナビノイドによって刈り込まれることにより、カラム状投射が完成することが示唆されました。カンナビノイド作動薬を腹腔内に投与すると、生後12日までの投与では変化は無かったにもかかわらず、生後13日以降では、カラム内外で均等に軸索長が短縮していました。またCB1R遺伝子をごく少数の細胞だけでノックアウトすると、その細胞特異的にカラム状投射が崩壊していました(図3)。
以上より、生後13日以降、軸索末端に発現するCB1Rによって、非自己カラムに侵入した軸索が選択的に刈り込まれることにより、カラム状投射が形成されることが明らかとなりました。
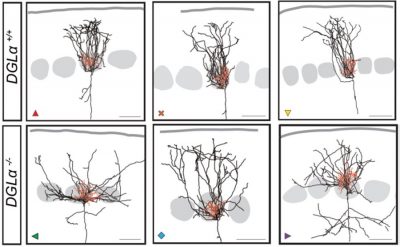 図2.内因性カンナビノイド欠失動物(DGLα-/-)では大脳皮質4層細胞のカラム状投射が崩壊する
図2.内因性カンナビノイド欠失動物(DGLα-/-)では大脳皮質4層細胞のカラム状投射が崩壊する
クリックで拡大表示します
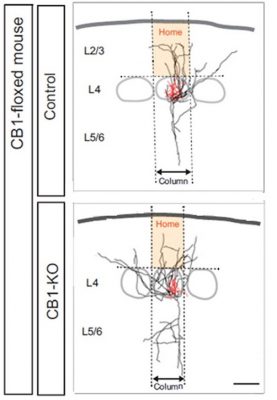 図3.CB1R遺伝子をノックアウト後、カラム状投射が崩壊した様子
図3.CB1R遺伝子をノックアウト後、カラム状投射が崩壊した様子
クリックで拡大表示します
本研究が社会に与える影響(本研究成果の意義)
本研究成果により、大脳皮質に広く共通する重要な構造の1つであるカラム状投射形成のメカニズムが初めて明らかにされました。これにより、大脳皮質の情報処理の共通原理の理解がさらに一歩進むと期待できます。また、カンナビノイドが緻密な神経回路形成に中心的な役割を果たす事が、またも明らかとなりました。同時に、ここではカンナビノイドが不要な投射を選択的に刈り込む事によって、正しい配線が出来上がることから、カンナビノイドが脳全体に広がるような、大麻の摂取では、神経線維が部位非特異的に広範に刈り込まれることが予測され、神経回路形成に重大な悪影響を与えることが示唆されます。
用語説明
※1 カンナビノイド
大麻(マリファナ)に含まれ、摂取による精神作用を起こす有効成分(テトラヒドロカンナビノール:Δ9-THC)と同様の作用を起こす化学物質類の総称。神経細胞に直接作用し、神経細胞間(シナプスでの情報伝達を阻害する。その受容体は脳内に広く存在する。その一方で、体内の代謝物として生産される「内因性カンナビノイドは、神経回路の形成や、情報伝達の制御に重要な役割を果たす。
特記事項
本研究成果は、2022年9月6日(火)午前4時(日本時間)に米国科学誌「米国科学アカデミー紀要(PNAS)」(オンライン)に掲載されました。
【タイトル】
“Endocannabinoid-dependent formation of columnar axonal projection in the mouse cerebral cortex”
【著者名】
Chiaki Itami1,2*, Naofumi Uesaka3, Jui-Yen Huang2, Hui-Chen Lu2, Kenji Sakimura4, Masanobu Kano3,5 and Fumitaka Kimura6,7* (*責任著者)
【所属】
- 埼玉医科大学医学部生理学教室
- Indiana Univ. Psychological and Brain Sciences
- 東京大学大学院医学系研究科神経生理学
- 新潟大学脳研究所細胞神経生物学
- 東京大学国際高等研究所ニューロインテリジェンス国際研究機構(WPI-IRCN)
- 大阪大学大学院医学系研究科 分子神経科学
- 滋慶医療科学大学医療科学部脳神経科学
【DOI番号】10.1073/pnas.2122700119










